题目内容
 2013年雾霾天气多次肆虐我国中东部地区.其中,汽车尾气和燃煤尾气是造成空气污染的原因之一.
2013年雾霾天气多次肆虐我国中东部地区.其中,汽车尾气和燃煤尾气是造成空气污染的原因之一.(1)汽车尾气净化的主要原理为:2NO(g)+2CO (g)
| 催化剂 |
①该反应的平衡常数表达式为
②该反应的△H
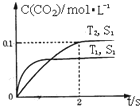
③当固体催化剂的质量一定时,增大其表面积可提高化学反应速率.若催化剂的表面积S1>S2,在右图中画出c(CO2)在T2、S2条件下达到平衡过程中的变化曲线.
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题.煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染.
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867kJ?mol-1
2NO2(g)?N2O4(g)△H=-56.9kJ?mol-1
写出CH4催化还原N2O4(g)生成N2(g)、CO2(g)和H2O(g)的热化学方程式
考点:物质的量或浓度随时间的变化曲线,用盖斯定律进行有关反应热的计算
专题:
分析:(1)①化学平衡常数为生成物浓度系数次幂的乘积与反应物浓度系数次幂乘积的比值,根据平衡常数的概念并结合反应方程式反应的平衡常数表达式;
②根据到达平衡的时间判断温度高低,根据平衡时二氧化碳的浓度判断温度对平衡的影响,进而判断△H;
③接触面积越大反应速率越快,到达平衡的时间越短,催化剂的表面积S1>S2,S2条件下达到平衡所用时间更长,但催化剂不影响平衡移动,平衡时二氧化碳的浓度与温度T1到达平衡时相同;
(2)根据盖斯定律,由已知热化学方程式乘以适当的系数进行加减构造目标热化学方程式.
②根据到达平衡的时间判断温度高低,根据平衡时二氧化碳的浓度判断温度对平衡的影响,进而判断△H;
③接触面积越大反应速率越快,到达平衡的时间越短,催化剂的表面积S1>S2,S2条件下达到平衡所用时间更长,但催化剂不影响平衡移动,平衡时二氧化碳的浓度与温度T1到达平衡时相同;
(2)根据盖斯定律,由已知热化学方程式乘以适当的系数进行加减构造目标热化学方程式.
解答:
解:(1)①2NO(g)+2CO (g)
2CO2 (g)+N2 (g)的平衡常数表达式为生成物浓度系数次幂的乘积与反应物浓度系数次幂乘积的比值,即:K=
,
故答案为:K=
;
②由图示可知,温度T1先到达平衡,故温度T1>T2,温度越高平衡时,二氧化碳的浓度越低,说明升高温度平衡向逆反应移动,故正反应为放热反应,即:△H<0,
故答案为:<;
③接触面积越大反应速率越快,到达平衡的时间越短,催化剂的表面积S1>S2,S2条件下达到平衡所用时间更长,但催化剂不影响平衡移动,平衡时二氧化碳的浓度与温度T1到达平衡时相同,故c(CO2)在T1、S2条件下达到平衡过程中的变化曲线为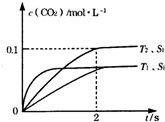 ,故答案为:
,故答案为: ;
;
(2)已知:①CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H1=-867kJ/mol
②2NO2(g)?N2O4(g)△H2=-56.9kJ/mol
根据盖斯定律,①-②得:CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g),故△H=-867kJ/mol-(-56.9kJ/mol)=-810.1kJ/mol,
即:CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g)△H=-810.1kJ/mol,
故答案为:CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g)△H=-810.1kJ/mol.
| 催化剂 |
| c2(CO2)?c(N2) |
| c2(NO)?c2(CO) |
故答案为:K=
| c2(CO2)?c(N2) |
| c2(NO)?c2(CO) |
②由图示可知,温度T1先到达平衡,故温度T1>T2,温度越高平衡时,二氧化碳的浓度越低,说明升高温度平衡向逆反应移动,故正反应为放热反应,即:△H<0,
故答案为:<;
③接触面积越大反应速率越快,到达平衡的时间越短,催化剂的表面积S1>S2,S2条件下达到平衡所用时间更长,但催化剂不影响平衡移动,平衡时二氧化碳的浓度与温度T1到达平衡时相同,故c(CO2)在T1、S2条件下达到平衡过程中的变化曲线为
 ,故答案为:
,故答案为: ;
;(2)已知:①CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H1=-867kJ/mol
②2NO2(g)?N2O4(g)△H2=-56.9kJ/mol
根据盖斯定律,①-②得:CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g),故△H=-867kJ/mol-(-56.9kJ/mol)=-810.1kJ/mol,
即:CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g)△H=-810.1kJ/mol,
故答案为:CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g)△H=-810.1kJ/mol.
点评:本题考查了物质的量浓度随时间变化的曲线、热化学方程式的书写,题目难度中等,注意掌握影响化学平衡的因素,明确盖斯定律的概念及应用方法,试题培养了学生灵活应用基础知识的能力.

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
已知常温下pH=3的醋酸溶液中存在电离平衡:CH3COOH?CH3COO-+H+要使溶液中的电离平衡发生移动,不可以采取的措施是( )
| A、加少量烧碱溶液 |
| B、加入浓度为0.001mol?L-1的HCl溶液 |
| C、加少量冰醋酸 |
| D、降低溶液的温度 |
下列物质中,既能跟盐酸反应,又能跟氢氧化钠反应的物质有( )
①Al ②Al2O3 ③Al(OH)3 ④(NH4)2SO4 ⑤Al2(SO4)3 ⑥KHCO3.
①Al ②Al2O3 ③Al(OH)3 ④(NH4)2SO4 ⑤Al2(SO4)3 ⑥KHCO3.
| A、①②③⑤ | B、②③④⑥ |
| C、①②③⑥ | D、①②③④⑥ |
已知常温下CH3COOH和NH3?H2O的电离常数相等,向10mL浓度为0.1mol/L的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中( )
| A、水的电离程度始终增大 | ||
B、
| ||
| C、c(CH3COOH)与c(CH3COO-)之和始终保持不变 | ||
| D、当加入氨水的体积为10 mL时,c(NH4+)=c(CH3COO-) |
下列叙述正确的是( )
| A、目前使用的元素周期表中,最长的周期含有36种元素 |
| B、周期表中所有元素都是从自然界中发现的,过渡元素都是金属元素 |
| C、非金属元素形成的共价化合物中,原子的最外层电子数只能是2或8 |
| D、IA族与VIIA族元素间可形成共价化合物或离子化合物 |
下列相应说法正确的是( )
| A、将城市的大型电镀工厂改建在农村,既促进农村经济发展又减轻城市用水污染 | ||||
| B、可吸入颗粒(例如硅酸盐粉尘)形成气溶胶,对人类健康危害极大 | ||||
| C、核裂变是一种化学变化 | ||||
D、核电站泄露的
|