题目内容
已知反应A+B=C+D的能量变化如图所示,下列说法正确的是( )


| A、该反应为放热反应 |
| B、该反应为吸热反应 |
| C、反应物的总能量低于生成物的总能量 |
| D、该反应只有在加热条件下才能进行 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:由图可知,反应物的总能量小于生成物的总能量,该反应为吸热反应,有的吸热反应常温下也能发生,据此分析.
解答:
解:A、依据图象分析,反应物的总能量低于生成物的总能量,所以反应是吸热反应,故A错误;
B、依据图象分析,反应物的总能量低于生成物的总能量,所以反应是吸热反应,故B正确;
C、依据图象分析,反应物的总能量低于生成物的总能量,故C正确;
D、有的吸热反应常温下也能发生,如铵盐与碱反应,所以该反应常温下也可能发生,故D错误;
故选BC.
B、依据图象分析,反应物的总能量低于生成物的总能量,所以反应是吸热反应,故B正确;
C、依据图象分析,反应物的总能量低于生成物的总能量,故C正确;
D、有的吸热反应常温下也能发生,如铵盐与碱反应,所以该反应常温下也可能发生,故D错误;
故选BC.
点评:本题考查了化学反应中能量的变化图,图象分析是解题关键,注意根据反应物的总能量与生成物的总能量进行比较,题目较简单.

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目
下列反应的离子方程式及对应的说法都正确的是( )
| A、碳酸氢钙溶液加到醋酸溶液中:Ca(HCO3)2+2CH3COOH═Ca2++2CH3COO-+2CO2↑+2H2O | ||||
B、用惰性电极电解氯化镁溶液:2Cl-+2H2O
| ||||
| C、电解精炼铜的阳极反应式只有:Cu-2e-=Cu2+ | ||||
| D、在氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O |
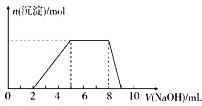 某溶液中可能含有如下离子:H+、Mg2+、Al3+、NH4+、Cl-、[Al(OH)4]-.当向该溶液中逐滴加入NaOH溶液时,产生沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示,下列说法正确的是( )
某溶液中可能含有如下离子:H+、Mg2+、Al3+、NH4+、Cl-、[Al(OH)4]-.当向该溶液中逐滴加入NaOH溶液时,产生沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示,下列说法正确的是( )| A、原溶液中一定含有的阳离子是H+、Mg2+、Al3+、NH4+ |
| B、反应最后形成的溶液中的溶质含AlCl3 |
| C、原溶液中Al3+与NH4+的物质的量之比为1:3 |
| D、原溶液中含有的阴离子是[Al(OH)4]-、Cl- |
3.04g铜镁合金完全溶解于含1.4mol HNO3的浓硝酸中,得到NO2和N2O4混合气体2240mL(标准状况下).向反应后的溶液中加入2mol/L NaOH溶液,当金属离子全部沉淀时,得到5.08g沉淀,下列说法正确的是( )
| A、该合金中镁与铜的物质的量之比是1:2 |
| B、NO2和N2O4的混合气体中,N2O4的体积分数是80% |
| C、得到5.08g沉淀时,加入NaOH溶液的体积是620mL |
| D、该反应中共转移电子为1.2NA |
 将锌棒和石墨棒按如图所示方式插入CuSO4溶液中,电流计指针发生偏转,下列针对该装置的说法正确的是( )
将锌棒和石墨棒按如图所示方式插入CuSO4溶液中,电流计指针发生偏转,下列针对该装置的说法正确的是( )| A、将电能转变为化学能 |
| B、电子由石墨棒流出 |
| C、锌为正极 |
| D、电池反应为:Zn+CuSO4═ZnSO4+Cu |
下列物质在指定的分散系中能大量共存的一组是( )
| A、空气:HCl、CO2、SO2、NH3 |
| B、水玻璃:K+、H+、NO3-、Cl |
| C、氨水:Na+、NH4+、NO3-、Al(OH)3 |
| D、pH=2的溶液:Fe2+、Ca2+、NO3-、Cl- |
配置100mL 1.0mol/L CuSO4溶液,下列有关说法正确的( )
| A、可选用250mL的容量瓶来配置 |
| B、配置过程中需要到胶头滴管 |
| C、用托盘天平称量溶质时,称量前指针向左偏,未调平即开始称量溶质,所配得的CuSO4溶液的浓度偏高 |
| D、需称取16g CuSO4?5H2O |
 在一个10L的密闭恒定温度的容器中加入1.0mol Z、1.0mol X、0mol Y开始反应,X、Y、Z三种物质物质的量随时间变化关系如图,在5min时Z、X、Y物质的量分别是0.1mol、0.7mol、0.6mol,下列说法正确的是( )
在一个10L的密闭恒定温度的容器中加入1.0mol Z、1.0mol X、0mol Y开始反应,X、Y、Z三种物质物质的量随时间变化关系如图,在5min时Z、X、Y物质的量分别是0.1mol、0.7mol、0.6mol,下列说法正确的是( )| A、前5min内,Z的平均反应速率是0.9 mol/(L?s) |
| B、该反应的化学方程式可表达式:2Y=3Z+X |
| C、在第2min时,Y和Z的物质的量浓度相等,表明反应处于平衡状态 |
| D、第5min后,X、Y、Z的浓度保持不变,正反应速率等于逆反应速率 |
成语言简意赅,是中华民族智慧的结晶.下列成语描绘的变化属于化学变化的是( )
| A、冰雪消融 | B、木已成舟 |
| C、蜡炬成灰 | D、沙里淘金 |