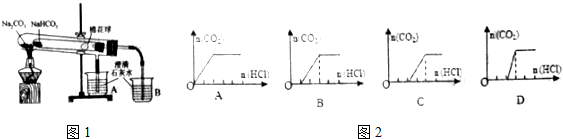
题目内容
4.室温下,某实验小组的同学将0.1mol/L的一元酸HA溶液和0.1mol/L的KOH溶液混合(忽略体积变化),实验数据如下表所示,下列判断一定正确的是( )| 实验编号 | 溶液体积(mL) | 反应后溶液的pH | |
| HA | KOH | ||
| ① | 10 | 10 | |
| ② | 10 | a | 7 |
| A. | 实验①所得的混合溶液中:c(K+)>c(A-)>c(H+)>c(OH-) | |
| B. | 实验①所得的混合溶液中:c(OH-)+c(A-)=c(K+)+c(H+) | |
| C. | 实验②所得的混合溶液中:c(A-)+c(HA)=0.1mol•L-1 | |
| D. | 实验②所得的混合溶液中:(K+)>c(A-)>c(OH-)=c(H+) |
分析 A.实验①所得的混合溶液的溶质为醋酸钾,醋酸根离子部分水解,溶液层碱性,则c(OH-)>c(H+);
B.根据醋酸钾溶液中的电荷守恒判断;
C.溶液的pH=7,则醋酸应该稍过量,结合物料守恒分析;
D.所得溶液为中性,则:c(K+)=c(A-)、c(OH-)=c(H+).
解答 解:A.等浓度、等体积的醋酸与氢氧化钾恰好完全反应生成醋酸钾,由于醋酸根离子部分水解,溶液层碱性,则c(OH-)>c(H+),正确的离子浓度大小为:c(K+)>c(A-)>c(OH-)>c(H+),故A错误;
B.实验①所得的混合溶液的溶质为醋酸钾,根据电荷守恒可得:c(OH-)+c(A-)=c(K+)+c(H+),故B正确;
C.实验②所得的混合溶液的pH=7,当两溶液体积相等时溶液呈碱性,若为中性,则醋酸应该稍过量,则混合液中0.1mol/L>c(A-)+c(HA)>0.05mol•L-1,故C错误;
D.实验②所得的混合溶液为中性,则:c(OH-)=c(H+),结合电荷守恒可知:c(K+)=c(A-),溶液中离子浓度大小为:c(K+)=c(A-)>c(OH-)=c(H+),故D错误;
故选B.
点评 本题考查了离子浓度大小比较,题目难度中等,明确溶液酸碱性与溶液pH的关系为解答结构,注意掌握电荷守恒、物料守恒及盐的水解原理的含义及应用方法,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
14.醇是重要的有机化工原料.一定条件下,甲醇可同时发生下面两个反应:
i.2CH3OH(g)?CH3OCH3(g)+H2O(g)
ii.2CH3OH(g)?C2H4(g)+H2O(g)
I.上述反应过程中能量变化如图所示:
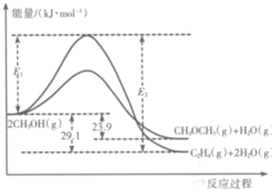
(1)在某密闭容器中,充人一定量CH3OH(g)发生上述两个反应,反应ⅰ(填“i”或“ii”)的速率较大,其原因为该反应的活化能较小.若在容器中加入催化剂,使ii的反应速率增大,则E1和E2-E1的变化是:
E1减小;E2-E1不变(填“增大”、“减小”或“不变”).
(2)已知:CH3CH2OH(g)=CH3OCH3(g)△H=+50.7kJ.mol-1.则乙烯气相直接水合反应C2H4(g)+H2O(g)=C2H5OH(g)的△H=-45.5 kJ•mol-1.
Ⅱ,某研究小组通过控制反应条件,在三个容积均为2L的密闭容器中只发生反应i,起始反应温度均为T℃,起始投料如下表所示:
(3)比较平衡时容器1中c1(H2O)和容器2中c2(H2O)的大小:c1(H2O)<c2(H2O)(填“>”、“<”或“=”);三个容器中反应的化学平衡常数分别记为K1、K2和K3,三者的大小关系为K1=K2>K3.
(4)若容器1中平衡时CH3OH(g)的转化率为80%,则该温度下反应i的平衡常数K=4.
i.2CH3OH(g)?CH3OCH3(g)+H2O(g)
ii.2CH3OH(g)?C2H4(g)+H2O(g)
I.上述反应过程中能量变化如图所示:

(1)在某密闭容器中,充人一定量CH3OH(g)发生上述两个反应,反应ⅰ(填“i”或“ii”)的速率较大,其原因为该反应的活化能较小.若在容器中加入催化剂,使ii的反应速率增大,则E1和E2-E1的变化是:
E1减小;E2-E1不变(填“增大”、“减小”或“不变”).
(2)已知:CH3CH2OH(g)=CH3OCH3(g)△H=+50.7kJ.mol-1.则乙烯气相直接水合反应C2H4(g)+H2O(g)=C2H5OH(g)的△H=-45.5 kJ•mol-1.
Ⅱ,某研究小组通过控制反应条件,在三个容积均为2L的密闭容器中只发生反应i,起始反应温度均为T℃,起始投料如下表所示:
起始投料/mol 编号 | CH3OH(g) | CH3OCH3(g) | H2O(g) |
| 恒温容器1 | 2 | 0 | 0 |
| 恒温容器2 | 0 | 2 | 2 |
| 绝热容器3 | 2 | 0 | 0 |
(4)若容器1中平衡时CH3OH(g)的转化率为80%,则该温度下反应i的平衡常数K=4.
15.工业上可利用图所示电解装置吸收和转化SO2(A、B均为惰性电极).下列说法正确的是( )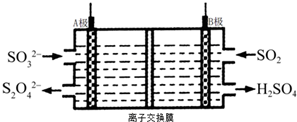

| A. | A电极接电源的正极 | |
| B. | A极区溶液的碱性逐渐增强 | |
| C. | 本装置中使用的是阴离子交换膜 | |
| D. | B极的电极反应式为SO2+2e-+2H2O═SO42-+4H+ |
13.下列物质不属于盐的是( )
| A. | 纯碱 | B. | KClO3 | C. | 小苏打 | D. | Na2O2 |
 到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源.
到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源.