题目内容
某温度下,重水D2O的离子积为1.6×10-15,若用pH一样的定义来规定pD=-lgc(D+),以下关于pD的叙述正确的是( )
| A、中性溶液的pD=7.0 |
| B、含0.01 mol的NaOH的D2O溶液1 L,其pD=12.0 |
| C、溶有0.01 mol DCl的水溶液1 L,其pD=2.0 |
| D、在100 mL 0.2 mol?L-1的DCl重水溶液中,加入100 mL 0.2 mol?L-1的NaOD的重水溶液,其pD=7.0 |
考点:水的电离,pH的简单计算
专题:电离平衡与溶液的pH专题
分析:A.根据重水D2O的离子积为1.6×10-15,结合pD=-lgc(D+)解答;
B.c(OD-)=10-2,根据c(D+)?c(OD-)=1.6×10-15,求c(D+)以及PD;
C.根据 pD=-lgc(D+),带入c(D+)=0.01mol/L进行求算;
D.先算出n(DC)、n(NaOD)的物质的量,判断反应后溶液酸碱性,在进行求算溶液的pD.
B.c(OD-)=10-2,根据c(D+)?c(OD-)=1.6×10-15,求c(D+)以及PD;
C.根据 pD=-lgc(D+),带入c(D+)=0.01mol/L进行求算;
D.先算出n(DC)、n(NaOD)的物质的量,判断反应后溶液酸碱性,在进行求算溶液的pD.
解答:
解:A.中性溶液中,重水电离出的重氢离子和重氢氧根离子浓度相等,重水(D2O)的离子积为c(D+)?c(OD-)=1.6×10-15,则c(D+)=c(OD-)=4×10-8mol/L,pD=-lgc(D+)=-lg4×10-8=8-2lg2,故A错误;
B.在1LD2O中溶解0.01mol NaOH(设溶液的体积为1L),则为0.01mol/LNaOH的D2O溶液,重水(D2O)的离子积为c(D+)?c(OH-)=1.6×10-15,c(D+)=
=1.6×1O-13,与pD=12,c(D+)=1×1O-12 mol/L矛盾,故B错误;
C.0.01mol DCl(设溶液的体积为1L),c(D+)=0.01mol/L,pD=-lgc(D+),把c(D+)=0.01mol/L带人后可以求得pD=-lgc(D+)=-lg10-2=2,故C正确;
D.n(DCl)=0.2mol/L×0.1L=0.02mol,n(NaOD)=0.2mol/L×0.1L=0.02mol,刚好完全反应,得到重水D2O的溶液,c(D+)=
mol/L,则pD不等于7,故D错误;
故选C.
B.在1LD2O中溶解0.01mol NaOH(设溶液的体积为1L),则为0.01mol/LNaOH的D2O溶液,重水(D2O)的离子积为c(D+)?c(OH-)=1.6×10-15,c(D+)=
| 1.6×10 -15 |
| 0.01 |
C.0.01mol DCl(设溶液的体积为1L),c(D+)=0.01mol/L,pD=-lgc(D+),把c(D+)=0.01mol/L带人后可以求得pD=-lgc(D+)=-lg10-2=2,故C正确;
D.n(DCl)=0.2mol/L×0.1L=0.02mol,n(NaOD)=0.2mol/L×0.1L=0.02mol,刚好完全反应,得到重水D2O的溶液,c(D+)=
| 1.6×10 -15 |
故选C.
点评:本题考查的是电离平衡知识的迁移应用,注意掌握溶液酸碱性与溶液pH的关系,注意利用pH计算方法进行计算该溶液的pD值,试题培养了学生的知识迁移能力,题目难度中等.

练习册系列答案
相关题目
垃圾资源化的方法是( )
| A、填埋 | B、焚烧 |
| C、堆肥 | D、分类回收 |
已知2Na2S+Na2SO3+3H2SO4=3S↓+3Na2SO4+3H2O,则反应中还原剂与还原产物的物质的量之比是( )
| A、2:1 | B、1:1 |
| C、1:2 | D、2:3 |
已知pKw=lgKw,如图表示某溶液中c(H+)和c(OH-)的关系,则有关判断错误的是( )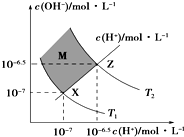

| A、两条曲线间任意点均有c(H+)×c(OH-)=KW |
| B、M区域内任意点对应的溶液均显酸性 |
| C、图中T1<T2 |
| D、XZ线上任意点均有pH=pKw/2 |
下列现象与原子核外电子跃迁无关的是( )
| A、激光 | B、焰火 |
| C、石墨导电 | D、霓虹灯光 |
下列有关原子结构或元素性质说法正确的是( )
| A、原子核外电子排布式为1s2的元素与原子核外电子排布式为1s22s2的元素化学性质相似 |
B、基态碳原子的价电子排布图: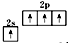 |
C、基态铜原子的价电子排布图: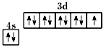 |
| D、Fe3+的最外层电子排布式为:3s23p63d5 |
下列离子方程式正确的是( )
| A、硫酸镁溶液跟氢氧化钡溶液反应:SO42-+Ba2+=BaSO4↓SO42- |
| B、H2SO4溶液与Ba(OH)2溶液反应:Ba2++OH-+H++=BaSO4↓+H2O |
| C、铜片插入硝酸银溶液中:Cu+2Ag+═Cu2++2Ag |
| D、澄清石灰水中加入盐酸 Ca(OH)2+2H+=Ca2++2H2O |
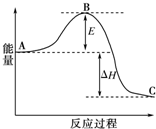 为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的反应热,并采取相应措施.化学反应的反应热通常用实验进行测定,也可进行理论推算.
为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的反应热,并采取相应措施.化学反应的反应热通常用实验进行测定,也可进行理论推算.