题目内容
15.研究证实,放射性元素${\;}_{53}^{125}$I可以治疗肿瘤,该元素原子的核内中子数是( )| A. | 72 | B. | 19 | C. | 53 | D. | 125 |
分析 元素符号的左上角为质量数、左下角为质子数,质量数=质子数+中子数,据此进行解答.
解答 解:放射性元素${\;}_{53}^{125}$I的质量数为125,质子数为53,则该原子的中子数为:125-53=72,
故选A.
点评 本题考查了核素组成及应用,题目难度不大,明确质量数与质子数、中子数之间的关系为解答关键,试题侧重基础知识的考查,培养了学生的灵活应用能力.

练习册系列答案
相关题目
5.能正确表示下列反应的离子方程式是( )
| A. | 铝放入烧碱溶液中溶解:2Al+2OH-+2 H2O═2 AlO2-+3H2↑ | |
| B. | 碳酸钙溶于醋酸溶液:CaCO3+2H+═Ca2++CO2↑+H2O | |
| C. | 稀硫酸中加氢氧化钡溶液至中性:H++OH-═H2O | |
| D. | NaHCO3溶液中加入稀盐酸:CO32-+2H+═CO2↑+H2O |
6. 金银花的有效成分为绿原酸,具有广泛的杀菌、消炎功能,其结构简式如图.下列有关绿原酸的说法中不正确的是( )
金银花的有效成分为绿原酸,具有广泛的杀菌、消炎功能,其结构简式如图.下列有关绿原酸的说法中不正确的是( )
 金银花的有效成分为绿原酸,具有广泛的杀菌、消炎功能,其结构简式如图.下列有关绿原酸的说法中不正确的是( )
金银花的有效成分为绿原酸,具有广泛的杀菌、消炎功能,其结构简式如图.下列有关绿原酸的说法中不正确的是( )| A. | 绿原酸分子中有4个手性碳原子(碳旁边连接4个不同的原子或原子团) | |
| B. | 绿原酸能发生显色反应、取代反应和加成反应 | |
| C. | 每摩尔绿原酸最多与4 mol NaOH反应 | |
| D. | 绿原酸分子中所有碳原子都能在同一平面上 |
3.现有如下各种说法,正确的是( )
①在水中氢、氧原子间均以化学键相结合
②金属元素的原子和非金属元素的原子化合均形成离子键
③离子键是阴、阳离子的相互吸引力
④根据电离方程式HCl═H++Cl-,判断HCl分子中存在离子键
⑤H2分子和Cl2分子的反应过程是H2、Cl2分子中共价键发生断裂生成H、Cl原子,而后H、Cl原子形成离子键的过程.
①在水中氢、氧原子间均以化学键相结合
②金属元素的原子和非金属元素的原子化合均形成离子键
③离子键是阴、阳离子的相互吸引力
④根据电离方程式HCl═H++Cl-,判断HCl分子中存在离子键
⑤H2分子和Cl2分子的反应过程是H2、Cl2分子中共价键发生断裂生成H、Cl原子,而后H、Cl原子形成离子键的过程.
| A. | ①②⑤正确 | B. | 都不正确 | ||
| C. | ④正确,其他不正确 | D. | 仅①不正确 |
10.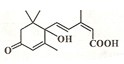 北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保持鲜花盛开.S-诱抗素的分子结构如图,下列关于该分子说法正确的是( )
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保持鲜花盛开.S-诱抗素的分子结构如图,下列关于该分子说法正确的是( )
 北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保持鲜花盛开.S-诱抗素的分子结构如图,下列关于该分子说法正确的是( )
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保持鲜花盛开.S-诱抗素的分子结构如图,下列关于该分子说法正确的是( )| A. | 其分子式为C15H20O4 | |
| B. | 该物质含三种官能团 | |
| C. | 能发生加成反应、取代反应、氧化反应、酯化反应、加聚反应 | |
| D. | 1mol该物质与足量NaOH溶液反应,最多消耗1molNaOH |
20.分子式为CnH2nO2的羧酸和某醇酯化生成分子式为Cn+2H2n+4O2的酯,反应所需羧酸和醇的质量比为1:1,则羧酸是( )
| A. | 甲酸 | B. | 乙酸 | C. | 丙酸 | D. | 乙二酸 |
7. 短周期元素甲、乙、丙、丁、戊、己、庚在周期表中的相对位置如图(甲不一定在丁、庚的连线上)戊、己分别是空气、地壳中含量最多的元素,下列判断正确的是( )
短周期元素甲、乙、丙、丁、戊、己、庚在周期表中的相对位置如图(甲不一定在丁、庚的连线上)戊、己分别是空气、地壳中含量最多的元素,下列判断正确的是( )
 短周期元素甲、乙、丙、丁、戊、己、庚在周期表中的相对位置如图(甲不一定在丁、庚的连线上)戊、己分别是空气、地壳中含量最多的元素,下列判断正确的是( )
短周期元素甲、乙、丙、丁、戊、己、庚在周期表中的相对位置如图(甲不一定在丁、庚的连线上)戊、己分别是空气、地壳中含量最多的元素,下列判断正确的是( )| A. | 甲一定是金属元素 | |
| B. | 气态氰化物的稳定性庚>己>戊 | |
| C. | 乙、丙、丁的最高价氧化物对应水化物可以相互反应 | |
| D. | 庚的最高价氧化物水化物酸性最强 |