题目内容
将MgCl2溶液加入NaOH和Na2CO3的混合液中,溶液中的离子反应如下:先发生Mg2++2OH-=Mg(OH)2↓,后发生Mg2++CO32-=MgCO3↓,经查溶解度表得知,Mg(OH)2的溶解度小于MgCO3的溶解度.
在溶解度表中有这样一组数据,表示四种物质在水中、液氨中的溶解度(g溶质/100g溶剂),如下表:
(1)分别是1.0mol?L-1的Ag+、Ba2+、NO3-和Cl-在水中发生反应的离子方程式是 .
(2)分别是0.50mol?L-1的以上四种离子在液氨中发生反应的离子方程式是 .
(3)得出以上结论的依据是 .
(4)将以上四种离子按适当浓度混合于液氨中,能否有AgCl沉淀析出?答: (“能”或“否”)
在溶解度表中有这样一组数据,表示四种物质在水中、液氨中的溶解度(g溶质/100g溶剂),如下表:
| 溶质 | AgNO3 | Ba(NO3)2 | AgCl | BaCl2 |
| 溶剂 | ||||
| 水 | 170 | 9.2 | 1.5×10-4 | 33.3 |
| 液氨 | 86 | 97.2 | 0.8 | 0 |
(2)分别是0.50mol?L-1的以上四种离子在液氨中发生反应的离子方程式是
(3)得出以上结论的依据是
(4)将以上四种离子按适当浓度混合于液氨中,能否有AgCl沉淀析出?答:
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:(1)据在水溶液中Ba(NO3)2和AgCl的浓度积小于其Ksp来分析;
(2)根据在液氨中,BaCl2的溶度积小于其Ksp来分析;
(3)若生成沉淀,则须浓度积Qc大于Ksp;
(4)四种离子按适当浓度混合于液氨中,由于在液氨中的溶解度Ba(NO3)2>AgNO3>AgCl>BaCl2,应首先考虑BaCl2的生成,再考虑AgCl的生成.
(2)根据在液氨中,BaCl2的溶度积小于其Ksp来分析;
(3)若生成沉淀,则须浓度积Qc大于Ksp;
(4)四种离子按适当浓度混合于液氨中,由于在液氨中的溶解度Ba(NO3)2>AgNO3>AgCl>BaCl2,应首先考虑BaCl2的生成,再考虑AgCl的生成.
解答:
解:(1)溶解度是指在某温度下,在100g水中达饱和时所能溶解的溶质的克数.
在水溶液中,
AgNO3的溶解度为170g,故在100g水中,当溶解170gAgNO3时达到饱和,170gAgNO3的物质的量n=
=1mol,故AgNO3的Ksp=C(Ag+)?C(Cl-)=10mol/L×10mol/L=100;
Ba(NO3)2的溶解度为9.2g,故在100g水中,当溶解9.2gBa(NO3)2时达到饱和,故Ba(NO3)2的物质的量n=0.035mol,故Ksp=C(Ba2+)?C2(NO3-)=0.35mol/L×(0.7mol/L)2=0.1715;
AgCl的溶解度为1.5×10-4g,故在100g水中,当溶解1.5×10-4gAgCl时达到饱和,故AgCl的物质的量n=1.05×10-6mol/mol,故AgCl的Ksp=C(Ag+)?C(Cl-)=1.05×10-5×1.05×10-5=1.1×10-10;
BaCl2的溶解度为33.3g,故在100g水中,当溶解33.3gBaCl2时达到饱和,故BaCl2的物质的量为0.16mol,故BaCl2的Ksp=C(Ba2+)?C2(Cl-)=1.6mol/L×(3.2mol/L)2=16.38
故在浓度分别是1.0mol?L-1的Ag+、Ba2+、NO3-和Cl-在水溶液中,Ba(NO3)2的浓度积Qc=C(Ba2+)?C2(NO3-)=1>Ba(NO3)2的Ksp,故会生成Ba(NO3)2,离子方程式为:Ba2++2NO3-=Ba(NO3)2↓;
AgCl的浓度积Qc=C(Ag+)?C(Cl-)=1>AgCl的Ksp,故会生成AgCl,离子方程式为:Ag++Cl-=AgCl↓;
故答案为:Ag++Cl-=AgCl↓,Ba2++2NO3-=Ba(NO3)2↓;
(2)在液氨中,
AgNO3的溶解度为86g,即在故在100g水中,当溶解86gAgNO3时达到饱和,86gAgNO3的物质的量为0.51mol,故故AgNO3的Ksp=C(Ag+)?C(Cl-)=5.1mol/L×5.1mol/L=25.1;
Ba(NO3)2的溶解度为97.2g,故在100g水中,当溶解97.2gBa(NO3)2时达到饱和,故Ba(NO3)2的物质的量n=0.37mol,故Ksp=C(Ba2+)?C2(NO3-)=3.7mol/L×(7.4mol/L)2=202.6;
BaCl2的溶解度为0g,故在100g水中,当溶解0gBaCl2时达到饱和,故BaCl2的物质的量为0.16mol,故BaCl2的Ksp=C(Ba2+)?C2(Cl-)=0,
浓度分别是0.50mol?L-1的以上四种离子混合时,由于BaCl2的Ksp=0,故Cl-首先与Ba2+生成BaCl2,离子方程式为:Ba2++2Cl-=BaCl2↓;
由于Cl-和Ba2+的浓度分别是0.50mol/L,故Ba2+能将Cl-沉淀完全至浓度为0,所以无AgCl沉淀生成.
故答案为:Ba2++2Cl-=BaCl2↓;
(3)当浓度积Qc大于Ksp时,会生成沉淀,故答案为:当浓度积Qc大于Ksp时,会生成沉淀;
(4)四种离子按适当浓度混合于液氨中,由于在液氨中的溶解度Ba(NO3)2>AgNO3>AgCl>BaCl2,应首先考虑BaCl2的生成,当Cl-过量,AgCl的Qc大于其Ksp时,会有AgCl的生成,故答案为:能.
在水溶液中,
AgNO3的溶解度为170g,故在100g水中,当溶解170gAgNO3时达到饱和,170gAgNO3的物质的量n=
| 170g |
| 170g/mol |
Ba(NO3)2的溶解度为9.2g,故在100g水中,当溶解9.2gBa(NO3)2时达到饱和,故Ba(NO3)2的物质的量n=0.035mol,故Ksp=C(Ba2+)?C2(NO3-)=0.35mol/L×(0.7mol/L)2=0.1715;
AgCl的溶解度为1.5×10-4g,故在100g水中,当溶解1.5×10-4gAgCl时达到饱和,故AgCl的物质的量n=1.05×10-6mol/mol,故AgCl的Ksp=C(Ag+)?C(Cl-)=1.05×10-5×1.05×10-5=1.1×10-10;
BaCl2的溶解度为33.3g,故在100g水中,当溶解33.3gBaCl2时达到饱和,故BaCl2的物质的量为0.16mol,故BaCl2的Ksp=C(Ba2+)?C2(Cl-)=1.6mol/L×(3.2mol/L)2=16.38
故在浓度分别是1.0mol?L-1的Ag+、Ba2+、NO3-和Cl-在水溶液中,Ba(NO3)2的浓度积Qc=C(Ba2+)?C2(NO3-)=1>Ba(NO3)2的Ksp,故会生成Ba(NO3)2,离子方程式为:Ba2++2NO3-=Ba(NO3)2↓;
AgCl的浓度积Qc=C(Ag+)?C(Cl-)=1>AgCl的Ksp,故会生成AgCl,离子方程式为:Ag++Cl-=AgCl↓;
故答案为:Ag++Cl-=AgCl↓,Ba2++2NO3-=Ba(NO3)2↓;
(2)在液氨中,
AgNO3的溶解度为86g,即在故在100g水中,当溶解86gAgNO3时达到饱和,86gAgNO3的物质的量为0.51mol,故故AgNO3的Ksp=C(Ag+)?C(Cl-)=5.1mol/L×5.1mol/L=25.1;
Ba(NO3)2的溶解度为97.2g,故在100g水中,当溶解97.2gBa(NO3)2时达到饱和,故Ba(NO3)2的物质的量n=0.37mol,故Ksp=C(Ba2+)?C2(NO3-)=3.7mol/L×(7.4mol/L)2=202.6;
BaCl2的溶解度为0g,故在100g水中,当溶解0gBaCl2时达到饱和,故BaCl2的物质的量为0.16mol,故BaCl2的Ksp=C(Ba2+)?C2(Cl-)=0,
浓度分别是0.50mol?L-1的以上四种离子混合时,由于BaCl2的Ksp=0,故Cl-首先与Ba2+生成BaCl2,离子方程式为:Ba2++2Cl-=BaCl2↓;
由于Cl-和Ba2+的浓度分别是0.50mol/L,故Ba2+能将Cl-沉淀完全至浓度为0,所以无AgCl沉淀生成.
故答案为:Ba2++2Cl-=BaCl2↓;
(3)当浓度积Qc大于Ksp时,会生成沉淀,故答案为:当浓度积Qc大于Ksp时,会生成沉淀;
(4)四种离子按适当浓度混合于液氨中,由于在液氨中的溶解度Ba(NO3)2>AgNO3>AgCl>BaCl2,应首先考虑BaCl2的生成,当Cl-过量,AgCl的Qc大于其Ksp时,会有AgCl的生成,故答案为:能.
点评:本题考查了沉淀的生成的条件,应注意若想生成沉淀,则须浓度积Qc大于Ksp,本题的难点在于由溶解度来计算难溶电解质的Ksp,把握住溶解度的概念是解题关键.

练习册系列答案
相关题目
下列有关有机化学实验说法正确的是( )
| A、用CCl4萃取溴水中的溴,可观察到溶液分层,上层为橙红色,下层接近无色 |
| B、石油的裂化、煤的液化和煤的气化都属于化学变化 |
| C、热的苯酚浓溶液放入冷水中冷却,溶液变浑浊,此时发生了化学反应 |
| D、往蛋白质溶液里加入饱和的CuSO4溶液,可提纯蛋白质 |
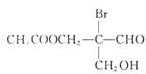 有机物若含手性碳原子(连接四个不同的原子或原子团的碳原子)就具有光学活性,如图物质发生下列反应后生成的有机物仍有光学活性的是( )
有机物若含手性碳原子(连接四个不同的原子或原子团的碳原子)就具有光学活性,如图物质发生下列反应后生成的有机物仍有光学活性的是( )①与甲酸、浓硫酸共热 ②与NaOH水溶液共热 ③与银氨溶液作用
④在Cu催化下与O2共热 ⑤在Ni催化下与氢气反应.
| A、仅③ | B、仅①③ |
| C、仅②④⑤ | D、①②③④⑤ |
下列叙述中,正确的是( )
| A、在AgBr饱和溶液中加入AgNO3溶液,达到平衡时,溶液中Br-浓度降低 |
| B、常温下,某溶液中由水电离出的c(OH-)=1×10-10mol/L,该溶液一定呈酸性 |
| C、FeCl3溶液和Fe2(SO4)3溶液加热蒸干,灼烧都得到Fe2O3 |
| D、向饱和碳酸钠溶液中通入足量二氧化碳,可以析出纯碱晶体 |
工业上利用N2和H2反应制取NH3,下列措施不能加快该反应的反应速率的是( )
| A、升高温度 |
| B、增大压强 |
| C、将NH3及时分离 |
| D、使用催化剂 |
