题目内容
有A、B、C、D四种金属,已知:只有D投入水中可与水剧烈反应;用B和C作电极,稀硫酸作电解质溶液构成原电池时,C为正极;A和C的离子共存于电解液中,以石墨为电极电解时阴极析出A.则这四种金属的活动性由强到弱的顺序是 .
考点:常见金属的活动性顺序及其应用,原电池和电解池的工作原理
专题:电化学专题
分析:金属越活泼,与水反应越剧烈;一般来说,作原电池负极的金属活动性较强;在电解池中,阴极上氧化性较强的离子先放电,金属离子的氧化性越强,对应的金属单质越不活泼,以此解答该题.
解答:
解:D投入水中可与水剧烈反应,说明D最活泼;
用B和C作电极,稀硫酸作电解质溶液构成原电池时,C为正极,说明金属的活动性B>C;
A和C的离子共存于电解液中,以石墨为电极电解时阴极析出A,说明金属活动性C>A;
则四种金属的活动性由强到弱的顺序是D>B>C>A,
故答案为:DBCA;
用B和C作电极,稀硫酸作电解质溶液构成原电池时,C为正极,说明金属的活动性B>C;
A和C的离子共存于电解液中,以石墨为电极电解时阴极析出A,说明金属活动性C>A;
则四种金属的活动性由强到弱的顺序是D>B>C>A,
故答案为:DBCA;
点评:本题以金属的活动性的比较为载体考查原电池和电解池知识,侧重于电极反应和放电顺序的考查,注意把握原电池和电解池的工作原理,学习中注意相关基础知识的积累,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
在不同反应中既能吸收CO2,又能参加反应放出CO2的是( )
| A、NaOH |
| B、Na2CO3 |
| C、NaHCO3 |
| D、Ca(OH)2 |
海南的水果大量向北方销售,运输这些水果时,常常将浸泡有高锰酸钾溶液的硅藻土放置在盛放水果的集装箱中,高锰酸钾溶液的作用是 ( )
| A、杀死水果周围的细菌,防止水果霉变 |
| B、吸收水果周围的氧气,防止水果腐烂 |
| C、吸收水果产生的乙烯,防止水果早熟 |
| D、发挥氧化性,催熟水果 |
解释下列物质性质的变化规律与物质结构间的因果关系时,与化学键强弱无关的变化规律是( )
| A、HF、HCI、HBr、HI的热稳定性依次减弱 |
| B、NaF、NaCl、NaBr、NaI的熔点依次降低 |
| C、F2、C12、Br2、I2的熔、沸点逐渐升高 |
| D、Li、Na、K、Rb 的熔点逐渐降低 |
下列反应中,属于加成反应的是( )
A、CH3CH2OH+CH3COOH
| |||
B、2CH3CHO+O2
| |||
| C、CH3-CH═CH2+Br2→CH3-CHBr-CH2Br | |||
D、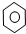 +Br2 +Br2
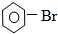 +HBr +HBr |
下列说法中正确的是( )
| A、摩尔是国际单位制中把宏观物质的质量与微观粒子的数目联系起来的一个物理量 |
| B、摩尔是物质的量的单位,简称摩,符号为mol |
| C、摩尔质量就是该物质的相对分子质量或相对原子质量 |
| D、阿伏加德罗常数为6.02×1023 |
常温下,下列溶液中可能大量共存的离子组是( )
| A、加入金属镁能产生H2的溶液中:Na+、Fe2+、SO42-、NO3- |
| B、含有大量Fe2+的溶液中:K+、Mg2+、ClO-、SO42- |
| C、能使Al3+生成沉淀的溶液中:NH4+、Na+、SiO32-、HCO3- |
| D、水电离产生的c(OH-)=1×10-10mol/L的溶液中:Al3+、SO42-、NO3-、Cl- |