题目内容
下列实验错误的是( )
| A、食醋用氢氧化钠溶液滴定,开始时溶液的pH通常变化缓慢,当接近滴定终点时,pH 出现突变,称为滴定突跃 |
| B、结晶时,若沉淀的结晶颗粒较大,静置后容易沉降到容器底部,此时,进行分离的操作方法是倾析 |
| C、抽滤装置由布氏漏斗、吸滤瓶、安全瓶、抽气泵等仪器组成,工作的主要原理是抽气泵给吸滤瓶减压,导致装置内部的压强降低,使过滤的速度加快 |
| D、在纸层析法分离Fe3+和Cu2+的实验中,层析后,经氨熏,滤纸中无色带出现,一定是误将试样点浸没在展开剂中 |
考点:化学实验方案的评价
专题:
分析:A.醋酸溶液中存在醋酸的电离平衡CH3COOH?CH3COO-+H+,滴定时氢离子被中和,氢离子浓度减小,电离平衡正移,所以溶液的PH变化缓慢;
B.沉淀的结晶颗粒较大,可用倾析分离;
C.减压过滤,利用大气压强原理,用减小压力的方法加快过滤的速率;
D.纸层析分离的基本原理是:亲脂性强的成分在流动相中分配的多一些,随流动相移动的速度就快一些;亲水性强的成分在固定相中分配的多一些,随流动相移动的速度就慢一些.
B.沉淀的结晶颗粒较大,可用倾析分离;
C.减压过滤,利用大气压强原理,用减小压力的方法加快过滤的速率;
D.纸层析分离的基本原理是:亲脂性强的成分在流动相中分配的多一些,随流动相移动的速度就快一些;亲水性强的成分在固定相中分配的多一些,随流动相移动的速度就慢一些.
解答:
解:A.醋酸溶液中存在醋酸的电离平衡CH3COOH?CH3COO-+H+,滴定时氢离子被中和,氢离子浓度减小,电离平衡正移,所以溶液的PH变化缓慢,故A正确;
B.沉淀的结晶颗粒较大,静置后容易沉降到容器底部,可用倾析分离,故B正确;
C.减压过滤,利用大气压强原理,用减小压力的方法加快过滤的速率,抽滤装置由布氏漏斗、吸滤瓶、安全瓶、抽气泵等仪器组成,故C正确;
D.展开剂选用不当造成的,可能造成滤纸中无色带出现,故D错误.
故选D.
B.沉淀的结晶颗粒较大,静置后容易沉降到容器底部,可用倾析分离,故B正确;
C.减压过滤,利用大气压强原理,用减小压力的方法加快过滤的速率,抽滤装置由布氏漏斗、吸滤瓶、安全瓶、抽气泵等仪器组成,故C正确;
D.展开剂选用不当造成的,可能造成滤纸中无色带出现,故D错误.
故选D.
点评:本题考查了中和滴定,物质的分离提纯,Cu2+与的性质等知识,比较基础,侧重对基础知识的巩固,注意对基础知识的理解掌握.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
用NA表示阿伏加德罗常数的值,下列叙述不正确的是( )
| A、1.6 g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA |
| B、0.1 mol H2O中含有电子的数目为NA |
| C、标准状况下,11.2L四氯化碳中含有分子的数目为0.5NA |
| D、0.5 mol?L-1 CaCl2溶液中的Cl-的数目为NA |
下列实验装置或操作正确的是( )
A、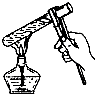 加热试管中的液体 |
B、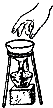 移走蒸发皿 |
C、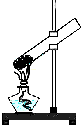 加热结晶水合物 |
D、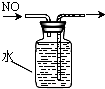 排水集气法收集NO |
下列各组物质的水溶液不用试剂无法鉴别出来的是( )
| A、NaOH、AlCl3 |
| B、CuSO4、BaCl2 |
| C、NaAlO2、HCl |
| D、MgCl2、AlCl3 |
下列说法或化学方程式正确的是( )
A、用坩埚灼烧MgCl2?6H2O的反应式:MgCl2?6H2O
| ||||
| B、在0.1mol?L-1 Na2SO3溶液中:c(Na+)=2c(SO32-)+c(HSO3-)+c(H2SO3) | ||||
| C、常温下,将PH=2的稀硫酸稀释10倍,其中各离子的浓度都变为原来的十分之一 | ||||
| D、蛋白质肽链中-NH-上的氢原子与羰基上的氧原子形成氢键是蛋白质二级结构的主要依据 |