题目内容
食品添加剂能提升各种食品的色香味,被誉为现代食品工业的灵魂,目前我国食品添加剂有23个类别,2000多个品种.
(1)作为酸度调节剂,下列物质中不宜直接食用的是 .
a盐酸 b乙酸 c乳酸 d氢氧化钠 e碳酸氢钠
(2)过氧化氢常作为袋装豆腐干的防腐剂,其电子式为 .
(3)食品抗结剂亚铁氰化钾[K4Fe(CN)6?3H2O]中,原子序数最大的元素位于元素周期表第 周期,其它元素的原子半径由大到小的顺序是 .
(4)碳酸钠可用作食品膨松剂,其水溶液中阴离子浓度由大到小的顺序是 .
(5)铁粉可作为食品脱氧剂.已知
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H1=一25kJ?mol一1;
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g)△H2=一47kJ?mol一1;
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g)△H3=+1 9kJ?mol一1.
用一氧化碳还原氧化亚铁制取铁粉的热化学方程式为 .
(1)作为酸度调节剂,下列物质中不宜直接食用的是
a盐酸 b乙酸 c乳酸 d氢氧化钠 e碳酸氢钠
(2)过氧化氢常作为袋装豆腐干的防腐剂,其电子式为
(3)食品抗结剂亚铁氰化钾[K4Fe(CN)6?3H2O]中,原子序数最大的元素位于元素周期表第
(4)碳酸钠可用作食品膨松剂,其水溶液中阴离子浓度由大到小的顺序是
(5)铁粉可作为食品脱氧剂.已知
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H1=一25kJ?mol一1;
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g)△H2=一47kJ?mol一1;
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g)△H3=+1 9kJ?mol一1.
用一氧化碳还原氧化亚铁制取铁粉的热化学方程式为
考点:常见的食品添加剂的组成、性质和作用,微粒半径大小的比较,用盖斯定律进行有关反应热的计算,盐类水解的应用,离子浓度大小的比较
专题:化学反应中的能量变化,元素周期律与元素周期表专题,盐类的水解专题,化学应用
分析:(1)根据选项中物质的性质进行解答;
(2)根据电子式的书写方法写出过氧化氢的电子式;
(3)亚铁氰化钾[K4Fe(CN)6?3H2O]中铁的原子序数最大;同周期自左而右原子半径减小,同主族自上而下原子半径增大;电子层越多半径越大,据此分析;
(4)碳酸钠电离出碳酸根离子和钠离子,碳酸根离子水解生成碳酸氢根离子和氢氧根离子,碳碳酸氢根离子水解生成碳酸和氢氧根离子,据此分析解答;
(5)依据盖斯定律构造目标方程式分析解答;
(2)根据电子式的书写方法写出过氧化氢的电子式;
(3)亚铁氰化钾[K4Fe(CN)6?3H2O]中铁的原子序数最大;同周期自左而右原子半径减小,同主族自上而下原子半径增大;电子层越多半径越大,据此分析;
(4)碳酸钠电离出碳酸根离子和钠离子,碳酸根离子水解生成碳酸氢根离子和氢氧根离子,碳碳酸氢根离子水解生成碳酸和氢氧根离子,据此分析解答;
(5)依据盖斯定律构造目标方程式分析解答;
解答:
解:(1)a盐酸是强酸,不能食用;b乙酸具有酸性和酸味,是常用的酸味剂和调味剂;c乳酸具有帮助消化、增进食欲的功能;d氢氧化钠是强碱具有腐蚀性,不能食用; e碳酸氢钠水溶液呈弱碱性,可作为酸度调节剂,
故答案为:ad;
(2)在过氧化氢分子中,一个过氧键:-O-O-(短线表示一对共用电子对),每个氧原子各连着1个氢原子,所以过氧化氢的电子式为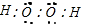 ,
,
故答案为: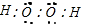 ;
;
(3)食品抗结剂亚铁氰化钾[K4Fe(CN)6?3H2O]中,原子序数分别为K:19;C:6;N:7;O:8;H:1;原子序数为26的铁元素原子序数最大,铁元素位于周期表第四周期第ⅤⅢ族;C、N、O都属于第二周期,具有相同电子层,且原子序数逐渐减大,故原子半径由大到小为C>N>O,K属于第四周期,H属于第一周期,所以原子半径由大到小的顺序是K>C>N>O>H,
故答案为:第四周期;K>C>N>O>H;
(4)碳酸钠是强碱弱酸盐,在溶液中电离出碳酸根离子和钠离子,碳酸根离子水解、CO32-+H2O?HCO3-+OH-、碳酸根离子水解生成碳酸氢根离子,碳酸氢根离子水解,HCO3-+H2O?H2CO3+OH-溶液呈碱性c(OH-)>c(H+),碳酸根离子的水解程度比碳酸氢根离子的大,但水解程度很小,故c(CO32-)>c(HCO3-),c(OH-)>c(HCO3-),
故答案为:c(CO32-)>c(OH-)>c(HCO3-);
(5)①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H1=一25kJ/mol;
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g)△H2=一47kJ/mol;
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g)△H3=+1 9kJ/mol;
依据盖斯定律
得到CO(g)+FeO(s)═Fe(s)+CO2(g)△H=一11kJ/mol;
故答案为:CO(g)+FeO(s)═Fe(s)+CO2(g)△H=一11kJ/mol;
故答案为:ad;
(2)在过氧化氢分子中,一个过氧键:-O-O-(短线表示一对共用电子对),每个氧原子各连着1个氢原子,所以过氧化氢的电子式为
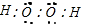 ,
,故答案为:
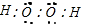 ;
;(3)食品抗结剂亚铁氰化钾[K4Fe(CN)6?3H2O]中,原子序数分别为K:19;C:6;N:7;O:8;H:1;原子序数为26的铁元素原子序数最大,铁元素位于周期表第四周期第ⅤⅢ族;C、N、O都属于第二周期,具有相同电子层,且原子序数逐渐减大,故原子半径由大到小为C>N>O,K属于第四周期,H属于第一周期,所以原子半径由大到小的顺序是K>C>N>O>H,
故答案为:第四周期;K>C>N>O>H;
(4)碳酸钠是强碱弱酸盐,在溶液中电离出碳酸根离子和钠离子,碳酸根离子水解、CO32-+H2O?HCO3-+OH-、碳酸根离子水解生成碳酸氢根离子,碳酸氢根离子水解,HCO3-+H2O?H2CO3+OH-溶液呈碱性c(OH-)>c(H+),碳酸根离子的水解程度比碳酸氢根离子的大,但水解程度很小,故c(CO32-)>c(HCO3-),c(OH-)>c(HCO3-),
故答案为:c(CO32-)>c(OH-)>c(HCO3-);
(5)①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H1=一25kJ/mol;
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g)△H2=一47kJ/mol;
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g)△H3=+1 9kJ/mol;
依据盖斯定律
| ①×3-【②+③×2】 |
| 6 |
故答案为:CO(g)+FeO(s)═Fe(s)+CO2(g)△H=一11kJ/mol;
点评:本题考查较为综合,考查了微粒半径的比较、过氧化氢的结构、离子浓度由大小比较、盖斯定律的应用,熟练构造目标方程式运用盖斯定律书写热化学方程式是解答本题的重点,题目难度中等.

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
白磷
黑磷,黑磷比白磷稳定,结构与石墨相似,下列叙述正确的( )
| 1215.9MPa,473K |
| A、黑磷与白磷互为同分异构体 |
| B、黑磷和白磷均不能导电 |
| C、白磷转化为黑磷是氧化还原反应 |
| D、白磷转化为黑磷是放热反应 |
用下列装置不能达到有关实验目的是( )

| A、用甲图装置电解精炼铝 |
| B、用乙图装置制备Fe(OH)2 |
| C、丙图装置酸性KMnO4溶液中出现气泡且颜色逐渐褪去 |
| D、用丁图装置验证NaHCO3和Na2CO3的热稳定性 |
金刚砂(SiC)可由SiO2和碳在一定条件下反应制得,反应方程式为SiO2+3C
SiC+2CO↑,下列有关制造金刚砂的说法中正确的是( )
| ||
| A、该反应中的氧化剂是SiO2,还原剂为C |
| B、该反应中的氧化产物和还原产物的物质的量之比为1:2 |
| C、该反应中转移的电子数为12e- |
| D、该反应中的还原产物是SiC、氧化产物是CO,其物质的量之比为1:2 |
[2012?济南调研]下列实验操作中,可以达到预期目的是( )
| A、用激光笔鉴别淀粉溶液和蔗糖溶液 |
| B、用过量的KSCN溶液除去FeCl2溶液中的少量FeCl3 |
| C、通过灼热的镁粉,可以除去N2中的少量O2 |
| D、用溶解、过滤的方法可分离Na2SO4和NaCl固体混合物 |
下列离子方程式正确的是( )
| A、明矾溶液中加入过量的氨水:Al3++4OH-═AlO2-+2H2O |
| B、漂白粉溶液中通入过量的二氧化碳:Ca2++2ClO-+CO2+H2O═CaCO3↓+2HClO+CO32- |
| C、FeBr2溶液中加入过量的氯水:2Br-+Cl2═Br2+2Cl- |
| D、澄清的石灰水中加入过量的NaHCO3溶液:Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32- |