题目内容
设NA代表阿伏加德罗常数,下列说法正确的是( )
| A、5.6 g铁与足量盐酸反应转移的电子数为0.2 NA |
| B、1mo1?L-1的AlC13溶液中,C1-离子的数目为3 NA |
| C、标准状况下,22.4 L氦气与22.4 L氯气所含原子数均为2 NA |
| D、60g二氧化硅与水反应生成硅酸的分子数为NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.铁与盐酸反应生成亚铁离子,0.1mol铁完全反应失去0.2mol电子;
B.缺少氯化铝溶液的体积,无法计算溶液中氯离子数目;
C.稀有气体为单原子分子,1mol氦气中含有1mol氦原子,而1mol氯气中含有2mol氯原子;
D.二氧化硅不与水发生反应,硅酸的分子数为0.
B.缺少氯化铝溶液的体积,无法计算溶液中氯离子数目;
C.稀有气体为单原子分子,1mol氦气中含有1mol氦原子,而1mol氯气中含有2mol氯原子;
D.二氧化硅不与水发生反应,硅酸的分子数为0.
解答:
解:A.5.6g铁的物质的量为0.1mol,0.1mol铁与足量盐酸完全反应生成0.1mol亚铁离子,失去0.2mol电子,反应转移的电子数为0.2NA,故A正确;
B.没有告诉氯化铝溶液的体积,无法计算溶液中氯离子的物质的量及数目,故B错误;
C.标况下22.4L氦气的物质的量为1mol,含有1mol氦原子,而22.4L氯气的物质的量为1mol,含有2mol氯原子,二者含有的原子数不相等,故C错误;
D.二氧化硅与水不会发生反应,无法计算生成硅酸的数目,故D错误;
故选A.
B.没有告诉氯化铝溶液的体积,无法计算溶液中氯离子的物质的量及数目,故B错误;
C.标况下22.4L氦气的物质的量为1mol,含有1mol氦原子,而22.4L氯气的物质的量为1mol,含有2mol氯原子,二者含有的原子数不相等,故C错误;
D.二氧化硅与水不会发生反应,无法计算生成硅酸的数目,故D错误;
故选A.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系;选项B为易错点,注意题中缺少溶液的体积.

练习册系列答案
相关题目
二氯化二硫(S2C12)可用作橡胶工业的硫化剂,常温下它是橙黄色有恶臭的液体,它的分子结构与H202相似,熔点为l93K,沸点为41lK,遇水很容易水解,产生的气体能使品红褪色,S2C12可由干燥的氯气通入熔融的硫中制得.下列有关说法正确的是( )
| A、S2C12晶体中不存在离子键 |
| B、S2C12分子中各原子均达到8电子稳定结构 |
| C、S2C12在熔融状态下能导电 |
| D、S2C12与水反应后生成的气体难溶于水 |
下列命名错误的是( )
| A、4-乙基-3-戊醇 |
| B、2-甲基-1-丁醇 |
| C、2-甲基-1-丙醇 |
| D、4-甲基-2-己醇 |
已知:2M(g)?N(g);△H<0.现将M和N的混和气体通入体积为1L的恒温密闭容器中,反应体系中物质浓度随时间变化关系如图所示.下列说法正确的是( )
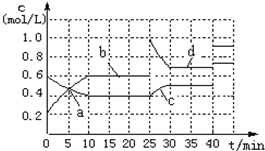

| A、a、b、c、d四个点中处于平衡状态的点是a、b |
| B、反应进行至25min时,曲线发生变化的原因是加入了 0.4molN |
| C、若调节温度使35min时体系内N的百分含量与15min时相等,应升高温度 |
| D、若40min后出现如图所示变化,则可能是加入了某种催化剂 |
X、Y为两种元素的原子,X的阴离子与Y的阳离子具有相同的电子层结构,由此可知( )
| A、X的原子半径大于Y的原子半径 |
| B、X的电负性小于Y的电负性 |
| C、X的氧化性大于Y的氧化性 |
| D、X的第一电离能小于Y的第一电离能 |
下列各组有机物中,两者一氯代物的种类相等的是( )
| A、正戊烷和正已烷 |
| B、对二甲苯和2,2-二甲基丙烷 |
| C、萘和乙烷 |
| D、甲苯和2-甲基丙烷 |
硫酸镁和硫酸铝溶液等体积混合后,Al3+浓度为0.1mol?L-1,SO42-浓度为0.3mol?L-1,则混合液中镁离了的浓度为( )
| A、0.45mol?L-1 |
| B、0.3mol?L-1 |
| C、0.15mol?L-1 |
| D、0.1mol?L-1 |
下列实验操作中,正确的是( )
| A、蒸发溶液时,边加热加搅拌,直至蒸发皿内的液体蒸干 |
| B、量取25.00LKMnO4溶液时,应选择酸式滴定管 |
| C、配制0.1mol/L的H2SO4溶液时,将量取的浓H2SO4注入容量瓶中加水稀释,边注入边搅拌 |
| D、配制一定物质的量浓度的溶液时,若未洗涤烧杯和玻璃棒,则会导致所配溶液的物质的量浓度偏高 |
向含n mol 硫酸铝的溶液中加入m mol NaOH溶液,观察到的现象是先有白色沉淀生成,后部分溶解,则生成Al(OH)3沉淀的物质的量是( )
| A、(8n-m)mol |
| B、(4m-n)mol |
| C、(4n-m)mol |
| D、(7n-m)mol |