题目内容
下列各物质所含原子个数按由大到小的顺序排列的是
①0.5molNH3 ②1molHe ③0.5molH2O ④0.2molH3PO4
A.①④③② B.④③②① C.②③④① D.①④②③
练习册系列答案
相关题目
14.根据下列操作及现象,所得结论正确的是( )
| 序号 | 操作及现象 | 结论 |
| A | 向溴水中加入少量苯,振荡静置后水层为无色 | 苯与Br2发生了加成反应 |
| B | 向某无色溶液中滴加硝酸酸化的BaCl2溶液,产生白色沉淀 | 原溶液中一定含有SO42- |
| C | 向25mL冷水和沸水中分别滴入5滴FeCl3饱和溶液,前者为黄色,后者为红褐色 | 温度升高,Fe3+的水解程度增大 |
| D | 将1mL KSCN溶液与1mL 同浓度FeCl3溶液充分混合;再继续加入KSCN溶液,溶液颜色加深 | 证明溶液中存在平衡:Fe3++3SCN?Fe(SCN)3 |
| A. | A | B. | B | C. | C | D. | D |
7.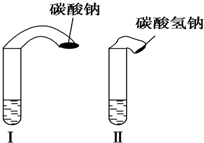 高中教材中有这样一个实验:在两支试管中分别加入3mL稀盐酸(均足量)(只有浓度小于1mol•L-1的稀盐酸跟Na2CO3和NaHCO3反应才能根据反应的剧烈程度区分开来,浓度较高则反应现象都是同样的剧烈),将两个各装有0.3g NaHCO3和Na2CO3粉末的小气球分别套在两支试管口上.将气球内的NaHCO3或NNa2CO3同时倒入试管中,观察到现象如下:
高中教材中有这样一个实验:在两支试管中分别加入3mL稀盐酸(均足量)(只有浓度小于1mol•L-1的稀盐酸跟Na2CO3和NaHCO3反应才能根据反应的剧烈程度区分开来,浓度较高则反应现象都是同样的剧烈),将两个各装有0.3g NaHCO3和Na2CO3粉末的小气球分别套在两支试管口上.将气球内的NaHCO3或NNa2CO3同时倒入试管中,观察到现象如下:
①试管中(填产生沉淀或气体及反应速率等相关现象)两支试管中都产生大量气泡,但盛NaHCO3的试管中反应速率要快得多;
②试管中气球大小(包含试管)体积之比约为(填最简单整数比)Ⅰ:Ⅱ=42:53;
③甲同学用手触摸试管,发现盛NaHCO3粉末的试管变凉,而盛Na2CO3粉末的试管温度有升高.由此他得出:不管其状态如何,NaHCO3和HCl反应为吸热反应,而Na2CO3和HCl反应为放热反应.
甲得出的结论是否正确不正确(填“正确”或“不正确”).
为研究是吸热反应还是放热反应,继续进行了下列实验(每次实验各做3次平行实验,取平均值):(注:每组固体全溶解且完全反应)
请你帮助填写相关内容:
(1)该研究报告的题目是《NaHCO3、Na2CO3和盐酸反应过程中热效应的研究》;
(2)该实验中所用的仪器除试管、药匙(或V形纸槽)、气球、下端带环状玻璃棒、烧杯、量筒、保温瓶外,还需要的仪器名称为托盘天平和温度计;
(3)通过上述实验可得出两条结论:
a.Na2CO3溶液和盐酸的反应是放热(吸热或放热)反应;
b.NaHCO3溶液和盐酸的反应是吸热(吸热或放热)反应.
 高中教材中有这样一个实验:在两支试管中分别加入3mL稀盐酸(均足量)(只有浓度小于1mol•L-1的稀盐酸跟Na2CO3和NaHCO3反应才能根据反应的剧烈程度区分开来,浓度较高则反应现象都是同样的剧烈),将两个各装有0.3g NaHCO3和Na2CO3粉末的小气球分别套在两支试管口上.将气球内的NaHCO3或NNa2CO3同时倒入试管中,观察到现象如下:
高中教材中有这样一个实验:在两支试管中分别加入3mL稀盐酸(均足量)(只有浓度小于1mol•L-1的稀盐酸跟Na2CO3和NaHCO3反应才能根据反应的剧烈程度区分开来,浓度较高则反应现象都是同样的剧烈),将两个各装有0.3g NaHCO3和Na2CO3粉末的小气球分别套在两支试管口上.将气球内的NaHCO3或NNa2CO3同时倒入试管中,观察到现象如下:①试管中(填产生沉淀或气体及反应速率等相关现象)两支试管中都产生大量气泡,但盛NaHCO3的试管中反应速率要快得多;
②试管中气球大小(包含试管)体积之比约为(填最简单整数比)Ⅰ:Ⅱ=42:53;
③甲同学用手触摸试管,发现盛NaHCO3粉末的试管变凉,而盛Na2CO3粉末的试管温度有升高.由此他得出:不管其状态如何,NaHCO3和HCl反应为吸热反应,而Na2CO3和HCl反应为放热反应.
甲得出的结论是否正确不正确(填“正确”或“不正确”).
为研究是吸热反应还是放热反应,继续进行了下列实验(每次实验各做3次平行实验,取平均值):(注:每组固体全溶解且完全反应)
| 序号 | 试剂1 | 试剂2 | 混合前 温度 | 混合后最高或 最低温度 |
| A | 50mL水 | 2.5g NaHCO3固体 | 20℃ | 18.5℃ |
| B | 50mL水 | 3.2g Na2CO3固体 | 20℃ | 23.3℃ |
| C | 50mL稀盐酸 | 2.5g NaHCO3固体 | 20℃ | 17.4℃ |
| D | 50mL稀盐酸 | 3.2g Na2CO3固体 | 20℃ | 24.4℃ |
(1)该研究报告的题目是《NaHCO3、Na2CO3和盐酸反应过程中热效应的研究》;
(2)该实验中所用的仪器除试管、药匙(或V形纸槽)、气球、下端带环状玻璃棒、烧杯、量筒、保温瓶外,还需要的仪器名称为托盘天平和温度计;
(3)通过上述实验可得出两条结论:
a.Na2CO3溶液和盐酸的反应是放热(吸热或放热)反应;
b.NaHCO3溶液和盐酸的反应是吸热(吸热或放热)反应.
4.烃A分子式为C4H10,分子结构中含有一个次甲基(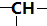 ),则此物质A的二溴代物的种数为( )
),则此物质A的二溴代物的种数为( )
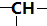 ),则此物质A的二溴代物的种数为( )
),则此物质A的二溴代物的种数为( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 以上都不对 |
5.将醋酸钠饱和溶液加热( )
| A. | 碱性增强 | B. | 碱性不变 | C. | pH不变 | D. | 碱性变弱 |


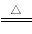 B+2C+2D,现测得分解产生的混合气体的密度是氢气的d倍,则A的相对分子量为
B+2C+2D,现测得分解产生的混合气体的密度是氢气的d倍,则A的相对分子量为