题目内容
2.t℃时,在体积不变的密闭容器中发生反应:X(g)+3Y(g)?2Z(g),各组分在不同时刻的浓度如表:( )
| 物质 | X | Y | Z |
| 初始浓度/mol•L-1 | 0.1 | 0.2 | 0 |
| 2 min末浓度/mol•L-1 | 0.08 | a | b |
| 平衡浓度/mol•L-1 | 0.05 | 0.05 | 0.1 |
| A. | 平衡时,X 的转化率为20% | |
| B. | t℃时,该反应的平衡常数为40 | |
| C. | 增大平衡后的体系压强,v正增大,v逆减小,平衡向正反应方向移动 | |
| D. | 前2 min 内,用Y 的变化量表示的平均反应速率v(Y)=0.03 mol•L-1•min-1 |
分析 A.平衡时X的浓度变化量为(0.1-0.05)mol/L=0.05mol/L,X转化率=$\frac{X浓度变化量}{X起始浓度}$×100%;
B.平衡常数表达式K=$\frac{{c}^{2}(Z)}{c(X)×{c}^{3}(Y)}$,代入平衡浓度计算;
C.增大压强,正逆反应速率都增大;
D.根据v=$\frac{△c}{△t}$计算v(X),再利用速率之比等于化学计量数之比计算v(Y).
解答 解:A.平衡时X的浓度变化量为(0.1-0.05)mol/L=0.05mol/L,X的转化率=$\frac{0.05mol/L}{0.1mol/L}$×100%=50%,故A错误;
B.平衡时X、Y均为0.05mol/L,Z为0.1mol/L,则平衡常数K=$\frac{{c}^{2}(Z)}{c(X)×{c}^{3}(Y)}$=$\frac{0.{1}^{2}}{0.05×0.0{5}^{3}}$=1600,故B错误;
C.增大压强,正逆反应速率都增大,正反应是气体体积减小的反应,增大压强平衡正向移动,正反应速率增大更多,故C错误;
D.前2 min内,v(X)=$\frac{(0.1-0.08)mol/L}{2min}$=0.01mol•L-1•min-1,速率之比等于化学计量数之比,则v(Y)=3v(X)=0.03mol•L-1•min-1,故D正确.故选D.
点评 本题考查较为综合,为高考常见题型,侧重于学生的分析能力和计算能力的考查,题目涉及合成平衡影响因素分析,平衡计算应用,转化率、平衡常数概念的分析计算应用,题目难度中等.

练习册系列答案
相关题目
15.下列有关溶液组成的描述合理的是( )
| A. | 无色溶液中可能大量存在Cu2+、K+、Cl?、NO3- | |
| B. | 酸性溶液中可能大量存在Na+、HCO3-、SO42?、I? | |
| C. | 碱性溶液中可能大量存在Na+、K+、Cl?、HCO3? | |
| D. | 中性溶液中可能大量存在Na+、K+、Cl?、SO42? |
13. 如图所示,图Ⅰ是恒压密闭容器,图Ⅱ是恒容密闭容器.当其它条件相同时,在Ⅰ、Ⅱ中都分别加入2molX和2molY,开始时容器的体积均为VL,发生如下反应并达到平衡状态:2X(?)+Y(?)?aZ(g).此时Ⅰ中X、Y、Z的物质的量之比为1:3:2.下列判断不正确的是( )
如图所示,图Ⅰ是恒压密闭容器,图Ⅱ是恒容密闭容器.当其它条件相同时,在Ⅰ、Ⅱ中都分别加入2molX和2molY,开始时容器的体积均为VL,发生如下反应并达到平衡状态:2X(?)+Y(?)?aZ(g).此时Ⅰ中X、Y、Z的物质的量之比为1:3:2.下列判断不正确的是( )
 如图所示,图Ⅰ是恒压密闭容器,图Ⅱ是恒容密闭容器.当其它条件相同时,在Ⅰ、Ⅱ中都分别加入2molX和2molY,开始时容器的体积均为VL,发生如下反应并达到平衡状态:2X(?)+Y(?)?aZ(g).此时Ⅰ中X、Y、Z的物质的量之比为1:3:2.下列判断不正确的是( )
如图所示,图Ⅰ是恒压密闭容器,图Ⅱ是恒容密闭容器.当其它条件相同时,在Ⅰ、Ⅱ中都分别加入2molX和2molY,开始时容器的体积均为VL,发生如下反应并达到平衡状态:2X(?)+Y(?)?aZ(g).此时Ⅰ中X、Y、Z的物质的量之比为1:3:2.下列判断不正确的是( )| A. | 物质Z的化学计量数a=1 | |
| B. | 若X、Y均为气态,则在平衡时X的转化率:Ⅰ>Ⅱ | |
| C. | 若Ⅱ中气体的密度变化如图Ⅲ所示,则X、Y中只有一种为气态 | |
| D. | 若X为固态、Y为气态,则Ⅰ、Ⅱ中从开始到平衡所需的时间:Ⅰ>Ⅱ |
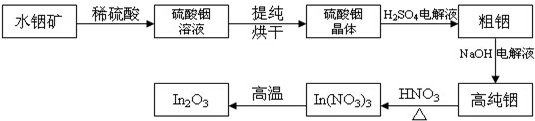
10.高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,不会造成二次污染.
己知高铁酸盐热稳定性差,工业上用湿法制备高铁酸钾的基本流程如图1所示:

(1)①上述氧化过程中,发生反应的离子方程式是2Fe3++3ClO-+10OH-=2FeO42-+3C1-+5H2O,在实际生产中一般控制反应温度30℃以下,其原因是防止生成的Na2FeO4发生分解.
②沉淀过程中加入浓KOH溶液可析出高铁酸钾(K2FeO4 ),这说明该温度下高铁酸钾的溶解度比高铁酸钠的溶解度小.
③在提纯K2FeO4中采用重结晶、洗涤、低温烘干的方法,沉淀洗涤方法是将沉淀置于漏斗中,让蒸馏水浸没沉淀,使水自然流下,重复操作2-3次.
④某温度下,将C12通入NaOH溶液中,反应后得到NaCl,NaC1O,NaClO3的混合溶液,经测定ClO-与C1O3-离子的物质的量之比是1:2,则C12与氢氧化钠反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为11:3.
(2)工业上还可用通过电解浓NaOH溶液制备Na2FeO4,其工作原理如图2所示:阳极的电极反应式为Fe-6e-+8OH-=FeO42-+4H2O,其中可循环使用的物质是NaOH溶液.
(3)CO2可转化为碳酸盐,其中Na2CO3是一种用途广泛的碳酸盐.
己知:25℃时,几种酸的电离平衡常数如表所示.
25℃时,向一定浓度的Na2CO3溶液中分别滴入等物质的量浓度的下列溶液至过量:
①NaHSO3②HNO3③HC1O,溶液中的n (HCO3-)与所加入溶液体积(V)的关系如图3所示.其中符合曲线Ⅱ的溶液为①③.
己知高铁酸盐热稳定性差,工业上用湿法制备高铁酸钾的基本流程如图1所示:

(1)①上述氧化过程中,发生反应的离子方程式是2Fe3++3ClO-+10OH-=2FeO42-+3C1-+5H2O,在实际生产中一般控制反应温度30℃以下,其原因是防止生成的Na2FeO4发生分解.
②沉淀过程中加入浓KOH溶液可析出高铁酸钾(K2FeO4 ),这说明该温度下高铁酸钾的溶解度比高铁酸钠的溶解度小.
③在提纯K2FeO4中采用重结晶、洗涤、低温烘干的方法,沉淀洗涤方法是将沉淀置于漏斗中,让蒸馏水浸没沉淀,使水自然流下,重复操作2-3次.
④某温度下,将C12通入NaOH溶液中,反应后得到NaCl,NaC1O,NaClO3的混合溶液,经测定ClO-与C1O3-离子的物质的量之比是1:2,则C12与氢氧化钠反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为11:3.
(2)工业上还可用通过电解浓NaOH溶液制备Na2FeO4,其工作原理如图2所示:阳极的电极反应式为Fe-6e-+8OH-=FeO42-+4H2O,其中可循环使用的物质是NaOH溶液.
(3)CO2可转化为碳酸盐,其中Na2CO3是一种用途广泛的碳酸盐.
己知:25℃时,几种酸的电离平衡常数如表所示.
| H2CO3 | H2SO3 | HNO2 | HClO |
| K1=4.4×10-7 K2=4.7×10-11 | K1=1.2×10-2 K2=6.6×10-8 | K=7.2×10-4 | K=2.9×10-8 |
①NaHSO3②HNO3③HC1O,溶液中的n (HCO3-)与所加入溶液体积(V)的关系如图3所示.其中符合曲线Ⅱ的溶液为①③.
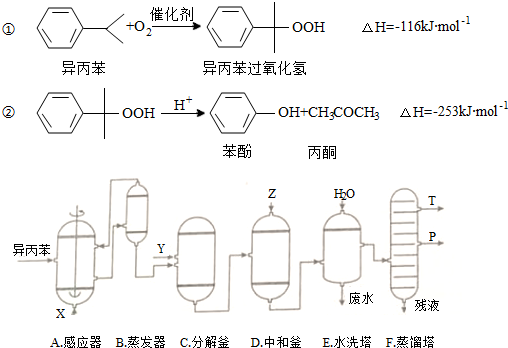
7.苯酚和丙酮都是重要的化工原料,工业上可用异丙苯氧化法生产苯酚和丙酮,其反应和工艺流程示意图如图:
相关化合物的物理常数
回答下列问题:
(1)在反应器A中通入的X是氧气或空气;
(2)反应①和②分别在装置A和C中进行(填装置符号).
(3)在分解釜C中加入的Y为少量浓硫酸,其作用是催化剂;
(4)中和釜D中加入的Z最适宜的是c(填编号.已知苯酚是一种弱酸)
a.NaOH b.CaCO3 c.NaHCO3 d.CaO
(5)蒸馏塔F中的馏出物T和P分别为丙酮和苯酚,判断的依据是丙酮的沸点低于苯酚;
(6)用该方法合成苯酚和丙酮的优点是原子利用率高.

相关化合物的物理常数
| 物质 | 相对分子质量 | 密度(g/cm-3) | 沸点/℃ |
| 异丙苯 | 120 | 0.8640 | 153 |
| 丙酮 | 58 | 0.7898 | 56.5 |
| 苯酚 | 94 | 1.0722 | 182 |
(1)在反应器A中通入的X是氧气或空气;
(2)反应①和②分别在装置A和C中进行(填装置符号).
(3)在分解釜C中加入的Y为少量浓硫酸,其作用是催化剂;
(4)中和釜D中加入的Z最适宜的是c(填编号.已知苯酚是一种弱酸)
a.NaOH b.CaCO3 c.NaHCO3 d.CaO
(5)蒸馏塔F中的馏出物T和P分别为丙酮和苯酚,判断的依据是丙酮的沸点低于苯酚;
(6)用该方法合成苯酚和丙酮的优点是原子利用率高.
14.某化学小组拟用环己醇制备环己烯.
【查阅资料】

【合成粗产品】
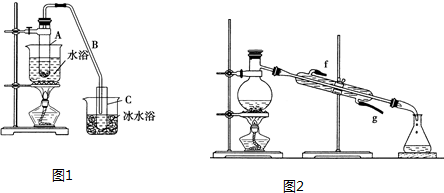
将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品.(图1)
(1)A中浓硫酸的作用是催化剂、脱水剂,将试管A置于水浴中的目的是冷却,防止环己烯挥发.
【精制粗产品】
(2)环己烯粗品中含有环己醇和少量酸性杂质等.加入c(填编号)洗涤,振荡、静置、分液,得到环己烯.
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
(3)将环己烯用图2装置进行蒸馏,该装置中还缺少的玻璃仪器是温度计,加热蒸馏前要先加入生石灰的目的是除去水.
(4)以下区分环己烯精品和粗品的方法,合理的是bc.
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点
【查阅资料】

| 密度(g•cm-3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品.(图1)
(1)A中浓硫酸的作用是催化剂、脱水剂,将试管A置于水浴中的目的是冷却,防止环己烯挥发.
【精制粗产品】
(2)环己烯粗品中含有环己醇和少量酸性杂质等.加入c(填编号)洗涤,振荡、静置、分液,得到环己烯.
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
(3)将环己烯用图2装置进行蒸馏,该装置中还缺少的玻璃仪器是温度计,加热蒸馏前要先加入生石灰的目的是除去水.
(4)以下区分环己烯精品和粗品的方法,合理的是bc.
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点

11.下列离子方程式书写错误的是( )
| A. | NaHSO3溶液与NaOH溶液反应:HSO3-+OH-═SO32-+H2O | |
| B. | 少量二氧化碳通入足量的NaOH溶液:CO2+2OH-═CO32-+H2O | |
| C. | Ba(OH)2与H2SO4反应:H++OH-═H2O | |
| D. | 氨水和醋酸溶液混合:NH3•H2O+CH3COOH═NH4++CH3COO-+H2O |