题目内容
不能说明醋酸是弱电解质的事实是( )
| A、醋酸溶液的导电性比盐酸弱 |
| B、向醋酸钠溶液中通入少量氯化氢,c(CH3COO-)减小 |
| C、0.1 mol/L的醋酸溶液的pH约为3 |
| D、pH=1的醋酸溶液用水稀释1000倍后,pH<4 |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:要证明醋酸为弱酸,可证明存在电离平衡、不能完全电离或从对应的强碱盐溶液呈碱性的角度,以此解答该题.
解答:
解:A.导电能力强弱与离子浓度大小有关,与电解质的强弱无关,故A错误;
B.醋酸钠溶液中存在水解平衡,向醋酸钠溶液中通入少量氯化氢,c(CH3COO-)减小,故B正确;
C.0.1 mol/L的醋酸溶液的pH约为3,说明醋酸部分电离,故C正确;
C.常温下,将pH=1的醋酸溶液稀释1000倍,测得pH<4,说明加水稀释促进电离,如为强酸,稀释后pH=4,可证明为弱酸,故D正确;
故选A.
B.醋酸钠溶液中存在水解平衡,向醋酸钠溶液中通入少量氯化氢,c(CH3COO-)减小,故B正确;
C.0.1 mol/L的醋酸溶液的pH约为3,说明醋酸部分电离,故C正确;
C.常温下,将pH=1的醋酸溶液稀释1000倍,测得pH<4,说明加水稀释促进电离,如为强酸,稀释后pH=4,可证明为弱酸,故D正确;
故选A.
点评:本题考查了弱电解质的判断,电解质强弱是根据其电离程度划分的,不能根据溶液导电性强弱划分,为易错点

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法符合第ⅦA族元素性质特征的是( )
| A、易形成-1价离子 |
| B、从上到下原子半径逐渐减小 |
| C、从上到下非金属性逐渐增强 |
| D、从上到下氢化物的稳定性依次减弱 |
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、标准状况下,2.24L甲醇中含有NA个碳原子 |
| B、在过氧化钠与水的反应中,每生成0.1 mol氧气,转移电子的数目为0.4 NA |
| C、常温常压下,1mol C10H22分子中含有共价键的数目为31NA |
| D、用含有0.1molFeCl3的饱和溶液制得的氢氧化铁胶体中胶粒数等于0.1NA |
下列叙述正确的是( )
| A、强电解质溶液的导电性不一定比弱电解质溶液的导电性强 |
| B、常温下,将pH=3的醋酸溶液稀释到原体积的10倍后,溶液的pH=4 |
| C、若测得雨水的pH小于7,则下的是酸雨 |
| D、在通风橱中进行有毒气体实验符合“绿色化学”思想 |
下列混合溶液中,各离子浓度的大小顺序正确的是( )
| A、10 mL 0.1 mol/L氨水与10 mL 0.1 mol/L盐酸混合,c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| B、10 mL 0.1 mol/L NH4Cl溶液与5 mL 0.2 mol/L NaOH溶液混合,c(Na+)=c(Cl-)>c(OH-)>c(H+) |
| C、10 mL 0.1 mol/L CH3COOH溶液与5 mL 0.2 mol/L NaOH溶液混合,c(Na+)=c(CH3COO-)>c(OH-)>c(H+) |
| D、10 mL 0.5 mol/L CH3COONa溶液与6 mL 1 mol/L盐酸混合,c(Cl-)>c(Na+)>c(OH-)>c(H+) |
下列各方程式中,属于水解反应的是( )
| A、HCO3-+H2O?H2CO3+OH- |
| B、HCO3-+H2O?CO32-+H3O+ |
| C、HCO3-+OH-?CO32-+H2O |
| D、CO32-+H+=HCO3- |
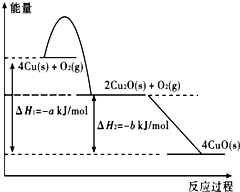 铜及其化合物在工业、农业、科技和日常生活中有广泛应用.
铜及其化合物在工业、农业、科技和日常生活中有广泛应用.