题目内容
把由CaCO3和MgCO3组成混合物充分加热至质量不在减少时,剩下的质量是原混合物质量的一半,计算原混合物中CaCO3和MgCO3的物质的量之比.
考点:有关混合物反应的计算
专题:计算题
分析:加热分解得到固体为CaO、MgO,令原混合物中CaCO3和MgCO3的物质的量分别为xmol、ymol,根据原子守恒表示出CaO、MgO的物质的量,再根据CaO、MgO质量之和等于CaCO3和MgCO3质量的一半列方程计算.
解答:
解:CaCO3和MgCO3组成混合物充分加热至质量不在减少时,得到固体为CaO、MgO,
令原混合物中CaCO3和MgCO3的物质的量分别为xmol、ymol,
根据Ca原子守恒,n(CaO)=n(CaCO3),根据Mg原子守恒n(MgO)=n(MgCO3),
则:2×(56x+40y)=100x+84y,整理得x:y=3:1,
答:原混合物中CaCO3和MgCO3的物质的量之比为3:1.
令原混合物中CaCO3和MgCO3的物质的量分别为xmol、ymol,
根据Ca原子守恒,n(CaO)=n(CaCO3),根据Mg原子守恒n(MgO)=n(MgCO3),
则:2×(56x+40y)=100x+84y,整理得x:y=3:1,
答:原混合物中CaCO3和MgCO3的物质的量之比为3:1.
点评:本题考查混合物计算,难度不大,明确发生的反应是解题关键,注意利用守恒法解答.

练习册系列答案
相关题目
下列离子方程式中,书写正确的是( )
| A、稀盐酸滴在铜片上:Cu+2H+=Cu2++H2↑ |
| B、氧化镁与稀硫酸混合:MgO+2H+=Mg2++H2O |
| C、铝片插入到硝酸银溶液中:Al+Ag+=Al3++Ag |
| D、稀盐酸滴在石灰石上:CaCO3+2H+=Ca2++H2CO3 |
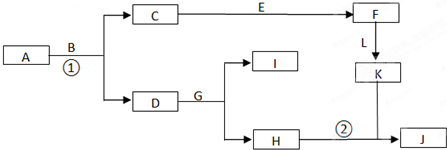
 某研究小组为了探究甲烷和氯气反应的情况,设计了几个实验.请填写下列空白:
某研究小组为了探究甲烷和氯气反应的情况,设计了几个实验.请填写下列空白: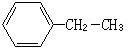
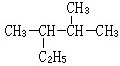
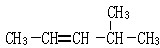
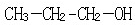 ;2-丙醇:
;2-丙醇: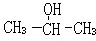 .
.