题目内容
8.下列关于SO2性质的说法正确的是( )| A. | 氯水中通入一定量的SO2气体可增强氯水的漂白性 | |
| B. | 因为SO2具有漂白性,所以它能使品红溶液、酸性高锰酸钾溶液褪色 | |
| C. | 已知酸性:H2SO4>HClO,则SO2通入漂白粉溶液中可生成次氯酸 | |
| D. | 紫色石蕊试液中通入SO2,溶液变红后不褪色 |
分析 A.氯气与二氧化硫等物质的量反应生成氯化氢和硫酸;
B.二氧化硫使品红溶液褪色体现其漂白性,使高锰酸钾褪色体现其还原性;
C.次氯酸具有强的氧化性,能够氧化亚硫酸;
D.二氧化硫为酸性氧化物,与水反应生成亚硫酸,具有酸性;二氧化硫不能漂白指示剂.
解答 解:A.氯气与二氧化硫等物质的量反应生成氯化氢和硫酸,氯化氢和硫酸不具有漂白性,所以氯水中通入一定量的SO2气体可减弱氯水的漂白性,故A错误;
B.二氧化硫使高锰酸钾褪色体现其还原性,故B错误;
C.次氯酸具有强的氧化性,能够氧化亚硫酸,则SO2通入漂白粉溶液中,不会生成次氯酸,故C错误;
D.二氧化硫为酸性氧化物,与水反应生成亚硫酸,具有酸性,能够使溶液变红后不褪色,故D正确;
故选:D.
点评 本题考查了二氧化硫的性质,熟悉二氧化硫漂白性、还原性、酸性氧化物的性质是解题关键,题目难度不大.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案
相关题目
18.下列叙述中,正确的是( )
| A. | 在多电子的原子里,能量高的电子通常在离核近的区域活动 | |
| B. | 核外电子总是先排在能量低的电子层上 | |
| C. | 两种微粒,若核外电子排布完全相同,则其化学性质一定相同 | |
| D. | 微粒的最外层只能是8个或2个电子才稳定 |
 )是一种可降解的聚酯类高分子材料,在材料的生物相容性方面有很好的应用前景.PPG的一种合成路线如下:
)是一种可降解的聚酯类高分子材料,在材料的生物相容性方面有很好的应用前景.PPG的一种合成路线如下: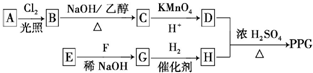
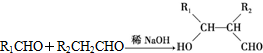

 .
. .
. .
.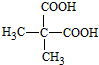
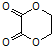 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2Br$→_{加热}^{NaOH/醇}$CH2=CH2$→_{催化剂}^{H_{2}O}$CH3CH2OH.
的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2Br$→_{加热}^{NaOH/醇}$CH2=CH2$→_{催化剂}^{H_{2}O}$CH3CH2OH.