题目内容
实验室常以天青石(主要成分为硫酸锶,含不溶性杂质)为原料制备碳酸锶(SrCO3).试回答下列问题:
(1)将天青石矿和炭混合后,高温焙烧过程中的产物为SrS(可溶于水)和CO,试写出该反应过程的化学方程式: .
(2)碳酸锶的另一种制备方法是用天青石和Na2CO3溶液混合浸泡制得,反应的离子方程式为SrSO4+CO32-?SrCO3+SO42-.
①若将Na2CO3换成(NH4)2CO3,则SrCO3的产率将降低,其原因是 .
②25℃时,对于浓度均为0.2mol?L-1的NaHCO3和Na2CO3溶液,下列判断中正确的是 .
A.均存在电离平衡和水解平衡
B.存在的粒子种类相同
C.溶液中阴离子的物质的量浓度之和:NaHCO3溶液>Na2CO3溶液
D.溶液中由水电离出的H+个数:Na2CO3溶液>NaHCO3溶液
(3)已知Ksp(SrSO4)=3×10-7,Ksp(SrCO3)=3×10-10,向1L SrCO3的饱和溶液中加入Na2SO4固体,当开始产生沉淀时,所需Na2SO4的质量为 .(假设溶液体积保持不变)
(1)将天青石矿和炭混合后,高温焙烧过程中的产物为SrS(可溶于水)和CO,试写出该反应过程的化学方程式:
(2)碳酸锶的另一种制备方法是用天青石和Na2CO3溶液混合浸泡制得,反应的离子方程式为SrSO4+CO32-?SrCO3+SO42-.
①若将Na2CO3换成(NH4)2CO3,则SrCO3的产率将降低,其原因是
②25℃时,对于浓度均为0.2mol?L-1的NaHCO3和Na2CO3溶液,下列判断中正确的是
A.均存在电离平衡和水解平衡
B.存在的粒子种类相同
C.溶液中阴离子的物质的量浓度之和:NaHCO3溶液>Na2CO3溶液
D.溶液中由水电离出的H+个数:Na2CO3溶液>NaHCO3溶液
(3)已知Ksp(SrSO4)=3×10-7,Ksp(SrCO3)=3×10-10,向1L SrCO3的饱和溶液中加入Na2SO4固体,当开始产生沉淀时,所需Na2SO4的质量为
考点:常见金属元素的单质及其化合物的综合应用
专题:元素及其化合物
分析:(1)由反应物、生成物及质量守恒定律分析;
(2)①Na2CO3换成(NH4)2CO3,则SrCO3的产率将降低,由SrSO4+CO32-?SrCO3+SO42-可知,与碳酸根离子浓度有关;
②A.任何溶液中均存在水的电离平衡,在水溶液中碳酸氢根存在电离平衡和水解平衡;
B.根据溶液中存在的微粒来回答;
C.碳酸根的水解程度大于碳酸氢根,水解规律:谁强显谁性;
D.碳酸氢根水解程度小;
(3)向1L SrCO3的饱和溶液中加入Na2SO4固体,发生SrCO3+SO42-?SrSO4+CO32-,Qc>Ksp生成沉淀.
(2)①Na2CO3换成(NH4)2CO3,则SrCO3的产率将降低,由SrSO4+CO32-?SrCO3+SO42-可知,与碳酸根离子浓度有关;
②A.任何溶液中均存在水的电离平衡,在水溶液中碳酸氢根存在电离平衡和水解平衡;
B.根据溶液中存在的微粒来回答;
C.碳酸根的水解程度大于碳酸氢根,水解规律:谁强显谁性;
D.碳酸氢根水解程度小;
(3)向1L SrCO3的饱和溶液中加入Na2SO4固体,发生SrCO3+SO42-?SrSO4+CO32-,Qc>Ksp生成沉淀.
解答:
解:(1)由反应物、生成物及质量守恒定律可知反应为4C+SrSO4
SrS+4CO↑,故答案为:4C+SrSO4
SrS+4CO↑;
(2)①当两者浓度相等时,Na2CO3溶液中c(CO32-)大于(NH4)2CO3溶液中c(CO32-),则由SrSO4+CO32-?SrCO3+SO42-可知,SrCO3的产率将降低,
故答案为:两者浓度相等时,Na2CO3溶液中c(CO32-)大于(NH4)2CO3溶液中c(CO32-),;
②A.Na2CO3溶液中存在水的电离平衡和碳酸根的水解平衡,NaHCO3在水溶液中存在碳酸氢根的电离平衡和水解平衡以及水的电离平衡,故A正确;
B.NaHCO3和Na2CO3溶液中存在的微粒均为:碳酸根、碳酸氢根、氢氧根、氢离子、碳酸分子、水分子,存在的粒子种类相同,故B正确;
C.等浓度时碳酸根离子水解程度大,则溶液中阴离子的物质的量浓度之和为NaHCO3溶液<Na2CO3溶液,故C错误;
D.等浓度时碳酸根离子水解程度大,碱性强,对水的促进程度大,则溶液中由水电离出的H+个数:Na2CO3溶液>NaHCO3溶液,故D正确;
故答案为:ABD;
(3)由Ksp(SrCO3)=3×10-10可知c(Sr2+)=
,当开始产生沉淀时,发生SrCO3+SO42-?SrSO4+CO32-,Qc>Ksp生成沉淀,c(SO42-)=
mol/L,则所需Na2SO4的质量为1L×
mol/L×142g/mol=2.46g,故答案为:2.46g.
| ||
| ||
(2)①当两者浓度相等时,Na2CO3溶液中c(CO32-)大于(NH4)2CO3溶液中c(CO32-),则由SrSO4+CO32-?SrCO3+SO42-可知,SrCO3的产率将降低,
故答案为:两者浓度相等时,Na2CO3溶液中c(CO32-)大于(NH4)2CO3溶液中c(CO32-),;
②A.Na2CO3溶液中存在水的电离平衡和碳酸根的水解平衡,NaHCO3在水溶液中存在碳酸氢根的电离平衡和水解平衡以及水的电离平衡,故A正确;
B.NaHCO3和Na2CO3溶液中存在的微粒均为:碳酸根、碳酸氢根、氢氧根、氢离子、碳酸分子、水分子,存在的粒子种类相同,故B正确;
C.等浓度时碳酸根离子水解程度大,则溶液中阴离子的物质的量浓度之和为NaHCO3溶液<Na2CO3溶液,故C错误;
D.等浓度时碳酸根离子水解程度大,碱性强,对水的促进程度大,则溶液中由水电离出的H+个数:Na2CO3溶液>NaHCO3溶液,故D正确;
故答案为:ABD;
(3)由Ksp(SrCO3)=3×10-10可知c(Sr2+)=
| 3×10-10 |
| 3×10-7 | ||
|
| 3×10-7 | ||
|
点评:本题考查金属及化合物的综合应用,为高频考点,把握氧化还原反应、盐类水解、溶度积的计算等为解答的关键,侧重分析与应用、计算能力的考查,题目难度不大.

练习册系列答案
相关题目
 一种从植物中提取的天然化合物M可用于制作香水,其结构简式如图所示,该化合物中不含的官能团是( )
一种从植物中提取的天然化合物M可用于制作香水,其结构简式如图所示,该化合物中不含的官能团是( )| A、碳碳双键 | B、羟基 |
| C、醛基 | D、羰基 |
将PH试纸测定浓H2SO4的PH值,试纸的颜色将变为( )
| A、蓝 | B、黑 | C、红 | D、白? |
如图所示实验不能达到实验目的是( )
A、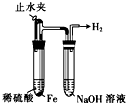 制备并观察氢氧化亚铁 |
B、 证明过氧化钠与水反应放热 |
C、 制备并收集少量NO2气体 |
D、 实验室制备少量氨气 |
用萃取法从碘水中分离出碘,所用萃取剂应具有的性质是( )
①不和碘水发生化学反应 ②能溶于水 ③应是极性溶剂 ④不溶于水 ⑤应是非极性溶剂.
①不和碘水发生化学反应 ②能溶于水 ③应是极性溶剂 ④不溶于水 ⑤应是非极性溶剂.
| A、①④⑤ | B、①③④ |
| C、①②⑤ | D、①②③ |
在铁酸钠(Na2FeO4)对来自河湖的淡水消毒是城市饮用水处理新技术,下列对Na2FeO4用于饮用水消毒处理的分析正确的是( )
| A、Na2FeO4在溶液中显强碱性,能消毒杀菌 |
| B、在Na2FeO4中Fe为+6价,具有强氧化性,能消毒杀菌 |
| C、Na2FeO4被水还原成Fe3+,Fe3+水解为Fe(OH)3胶体,可使水中悬浮物凝聚沉降 |
| D、Na2FeO4的还原产物是Fe2+,易水解为Fe(OH)2,可使水中悬浮物凝聚沉降 |
能用离子方程式H++OH-=H2O来表示的化学反应是( )
| A、氢氧化镁和盐酸反应 |
| B、硫酸和氢氧化钡溶液反应 |
| C、氢氧化铜和盐酸反应 |
| D、氢氧化钾溶液和盐酸反应 |
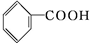 )和碱石灰的混合物得到液体,命名为苯.写出苯甲酸钠与碱石灰共热生成苯的化学方程式:
)和碱石灰的混合物得到液体,命名为苯.写出苯甲酸钠与碱石灰共热生成苯的化学方程式: NH4Al(SO4)2是加工食品最为快捷的食品添加剂,用于焙烤食品;NH4HSO4在分析试剂、医药、电子工业有广泛应用.试回答下列问题:
NH4Al(SO4)2是加工食品最为快捷的食品添加剂,用于焙烤食品;NH4HSO4在分析试剂、医药、电子工业有广泛应用.试回答下列问题: