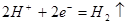题目内容
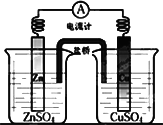
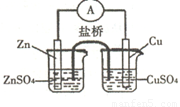
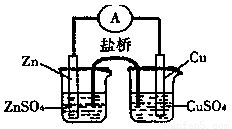
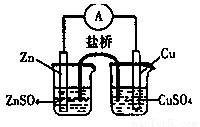
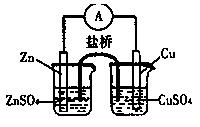
关于下图所示的原电池,下列说法正确的是
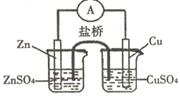
- A.电子从锌电极通过电流表流向铜电极
- B.盐桥中的阴离子向硫酸铜溶液中迁移
- C.取出盐桥后,电流计的指针仍发生偏转
- D.铜电极上发生的电极反应是2H+ + 2e- = H2↑
A
试题分析:原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应锌比铜活泼,所以根据装置图可知,锌是负极,失去电子,则电子从锌电极通过电流表流向铜电极,A正确。B不正确,盐桥中的阴离子向硫酸锌溶液中迁移;取出盐桥后,形成断路,不能构成原电池,电流计的指针不能发生偏转,C不正确;铜电极上发生的电极反应是Cu2++2e-=Cu,D不正确,答案选A。
考点:考查原电池的有关判断
点评:该题是高考中的常见题型,属于中等难度的试题。该题的关键是明确原电池的工作原理,特别是电极名称的判断、电极反应式的书写,然后结合题意和装置图灵活运用即可。
试题分析:原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应锌比铜活泼,所以根据装置图可知,锌是负极,失去电子,则电子从锌电极通过电流表流向铜电极,A正确。B不正确,盐桥中的阴离子向硫酸锌溶液中迁移;取出盐桥后,形成断路,不能构成原电池,电流计的指针不能发生偏转,C不正确;铜电极上发生的电极反应是Cu2++2e-=Cu,D不正确,答案选A。
考点:考查原电池的有关判断
点评:该题是高考中的常见题型,属于中等难度的试题。该题的关键是明确原电池的工作原理,特别是电极名称的判断、电极反应式的书写,然后结合题意和装置图灵活运用即可。

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
|
关于下图所示的原电池,下列说法正确的是
| |
| [ ] | |
A. |
电流从锌电极通过检流计流向铜电极 |
B. |
盐桥中的阳离子向硫酸铜溶液中迁移 |
C. |
锌电极发生还原反应,铜电极发生氧化反应 |
D. |
铜电极上发生的电极反应是2H++e-=H2↑ |