题目内容
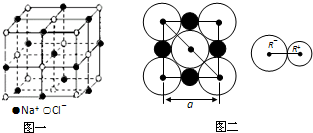
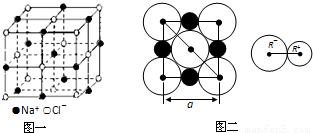
晶胞是晶体中最小的重复单位,数目巨大的晶胞无隙并置构成晶体.NaCl晶体是一个正六面体(如图一).我们把阴、阳离子看成不等径的圆球,并彼此相切(已知a为常数).

请计算下列问题:
(1)每个晶胞平均分摊
(2)NaCl晶体中阴阳离子的最短距离为
(用a表示).
(3)NaCl晶体为“巨分子”,在高温下(≥1413℃时)晶体转变成气态团簇分子.现有1molNaCl晶体,加强热使其气化,测得气体体积为11.2L(已折算为标准状况).则此时氯化钠气体的分子式为

请计算下列问题:
(1)每个晶胞平均分摊
4
4
个Na+,4
4
个Cl-.(2)NaCl晶体中阴阳离子的最短距离为
| a |
| 2 |
| a |
| 2 |
(3)NaCl晶体为“巨分子”,在高温下(≥1413℃时)晶体转变成气态团簇分子.现有1molNaCl晶体,加强热使其气化,测得气体体积为11.2L(已折算为标准状况).则此时氯化钠气体的分子式为
Na2Cl2
Na2Cl2
.分析:(1)利用均摊法计算每个晶胞中含有的氯离子和钠离子个数;
(2)根据图片二确定NaCl晶体中阴阳离子的最短距离;
(3)M=
=
,根据摩尔质量确定其化学式.
(2)根据图片二确定NaCl晶体中阴阳离子的最短距离;
(3)M=
| m |
| n |
| m | ||
|
解答:解:(1)该晶胞中钠离子个数=12×
+1=4,氯离子个数=8×
+6×
=4;
故答案为:4,4;
(2)根据图片二知,NaCl晶体中阴阳离子的最短距离为a的一半即
;
故答案为:
;
(3)1mol氯化钠的质量=1mol×58.8g/mol=58.5g,标况下,气体体积为11.2L的氯化钠的物质的量=
=0.5mol,M=
=117g/mol,所以氯化钠气体的分子式为Na2Cl2;
故答案为:Na2Cl2.
| 1 |
| 4 |
| 1 |
| 8 |
| 1 |
| 2 |
故答案为:4,4;
(2)根据图片二知,NaCl晶体中阴阳离子的最短距离为a的一半即
| a |
| 2 |
故答案为:
| a |
| 2 |
(3)1mol氯化钠的质量=1mol×58.8g/mol=58.5g,标况下,气体体积为11.2L的氯化钠的物质的量=
| 11.2L |
| 22.4L/mol |
=0.5mol,M=
| 58.5g |
| 0.5mol |
故答案为:Na2Cl2.
点评:本题考查了晶胞的计算、化学式的确定等知识点,根据均摊法计算晶胞中离子个数、根据摩尔离子确定化学式来分析解答即可,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
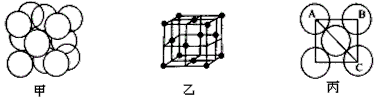
 ,试求铁金属晶体中的晶胞长度,即下图 丙中AB的长度为______________m.
,试求铁金属晶体中的晶胞长度,即下图 丙中AB的长度为______________m.
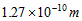 ,试求铁金属晶体中的晶胞长度,即下图丙中AB的长度为
,试求铁金属晶体中的晶胞长度,即下图丙中AB的长度为