题目内容
19.NA为阿伏伽德罗常数的值.下列说法正确的是( )| A. | 1 molCu和足量热浓硫酸反应可生成NA个SO3分子 | |
| B. | 3mol单质Fe完全转变为Fe3O4,失去8 NA个电子 | |
| C. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.4NA | |
| D. | 密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA |
分析 A.铜与浓硝酸反应生成的是二氧化硫;
B.根据Fe3O4中铁为+$\frac{8}{3}$价来分析;
C.过氧化钠与水反应时,氧元素的价态由-1价变为0价;
D.NO2和N2O4之间存在转化,方程式2NO2?N2O4.
解答 解:A.1molCu和足量热浓硫酸反应生成1mol二氧化硫,不会生成三氧化硫,故A错误;
B.Fe3O4中铁为+$\frac{8}{3}$价,故1mol铁反应失去$\frac{8}{3}$mol电子,3mol单质Fe完全转化为Fe3O4失去8mol电子,即8NA个,故B正确;
C.过氧化钠与水反应时,氧元素的价态由-1价变为0价,故当生成0.1mol氧气时转移0.2mol电子即0.2NA个,故C错误;
D.NO和O2反应方程式为2NO+O2=2NO2,根据方程式知,2molNO与1molO2恰好完全反应生成2molNO2,但NO2和N2O4之间存在转化,方程式2NO2?N2O4,所以产物分子数小于2NA,故D错误;
故选:B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大,注意过氧化钠与水反应中氧元素化合价变化.

练习册系列答案
相关题目
10.根据下列实验操作和现象所得出的结论错误的是( )
| 选项 | |||
| A | 向蔗糖中加入浓硫酸 | 蔗糖变成疏松多孔的海绵状碳 | 浓硫酸具有脱水性和强氧化性 |
| B | 向盛有Na2SiO3溶液的试管中滴加1滴酚酞,然后逐滴加入稀盐酸至红色退去 | 2min后,试管里出现凝胶 | 非金属性:Cl>Si |
| C | 向盛有铜片的容器中加入浓硝酸 | 产生大量红棕色气体,溶液变为蓝绿色 | 浓硝酸具有强氧化性和酸性 |
| D | 向浓度均为KCl、KI混合溶液中滴加少量AgNO3溶液 | 先出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| A. | A | B. | B | C. | C | D. | D |
10.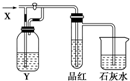 如图:是一套检验气体性质的实验装置.向装置中缓慢通入气体X,若关闭活塞,则品红溶液无变化而澄清的石灰水变浑浊;若打开活塞,则品红溶液褪色.据此判断气体X和洗气瓶内溶液Y分别可能为( )
如图:是一套检验气体性质的实验装置.向装置中缓慢通入气体X,若关闭活塞,则品红溶液无变化而澄清的石灰水变浑浊;若打开活塞,则品红溶液褪色.据此判断气体X和洗气瓶内溶液Y分别可能为( )
 如图:是一套检验气体性质的实验装置.向装置中缓慢通入气体X,若关闭活塞,则品红溶液无变化而澄清的石灰水变浑浊;若打开活塞,则品红溶液褪色.据此判断气体X和洗气瓶内溶液Y分别可能为( )
如图:是一套检验气体性质的实验装置.向装置中缓慢通入气体X,若关闭活塞,则品红溶液无变化而澄清的石灰水变浑浊;若打开活塞,则品红溶液褪色.据此判断气体X和洗气瓶内溶液Y分别可能为( )| A | B | C | D | |
| X | SO2 | SO2 | CO2 | Cl2 |
| Y | 饱和的NaHCO3溶液 | 浓硫酸 | Na2SO3 溶液 | Na2CO3溶液 |
| A. | A | B. | B | C. | C | D. | D |
7.可逆反应:2A(g)+2B(g)?C(g)+3D(g) 在不同情况下测得下列4种反应速率,其中反应最快的是( )
| A. | v(A)=0.45mol/(L•s) | B. | v(B)=0.6mol/(L•s) | C. | v(C)=0.5mol/(L•min) | D. | v(D)=0.4mol/(L•s) |
14.下列电子式书写正确的是( )
| A. | 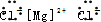 | B. |  | C. | 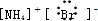 | D. | 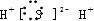 |
11.一定由两种元素组成的物质是( )
| A. | 氧化物 | B. | 酸 | C. | 碱 | D. | 盐 |
8.已知:4NH3(g)+5O2(g)?4NO(g)+6H2O(g),若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则下列关系不正确的是( )
| A. | 4v(NH3)=5v(O2) | B. | 6v(O2)=5v(H2O) | C. | 3v(NH3)=2v(H2O) | D. | 4v(O2)=5v(NO) |
9.既能与盐酸反应,又能与NaOH溶液反应的是( )
①Al;②Al(OH)3;③(NH4)2CO3;④Na2CO3;⑤NaHCO3;⑥NaHSO4.
①Al;②Al(OH)3;③(NH4)2CO3;④Na2CO3;⑤NaHCO3;⑥NaHSO4.
| A. | ②③⑤ | B. | ①②③⑤ | C. | ②③④⑤ | D. | ②③④⑤⑥ |