题目内容
往一体积不变的密闭容器中充入H2和I2,发生反应H2 (g)+I2 (g)?2HI(g)△H<0,当达到平衡后,t0时刻改变某一条件(混合气体量不变),容器内压强增大,下列说法正确的是( )
| A、可能为升温 |
| B、平衡一定不移动 |
| C、H2 转化率增大 |
| D、HI平衡浓度一定变大 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:该反应为反应前后气体体积不变的放热反应,混合气体的物质的量不变而容器内压强增大,只能是升高了温度,导致气体压强增大.
解答:
解:该反应为反应前后气体体积不变的放热反应,混合气体的物质的量不变而容器内压强增大,只能是升高温度,导致气体压强增大;升温平衡逆向移动,氢气转化率减小,HI平衡浓度减小,
故选A.
故选A.
点评:本题考查化学反应速率与化学平衡的影响因素,判断改变的条件为升高温度是解题的关键,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
某温度下,在一容积可变的密闭容器里,反应2A(g)?B(g)+2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol、4mol.在保持温度和压强不变的条件下,下列说法正确的是( )
| A、充入1mol稀有气体氦(He),平衡将向正反应方向移动 |
| B、充入A、B、C各1mol,平衡将向正反应方向移动 |
| C、将A、B、C各物质的量都减半,C的百分含量变大 |
| D、加入一定量的A气体达平衡后,C的百分含量一定增加 |
下列说法正确的是( )
| A、乙烯、氯乙烯、聚乙烯均可使酸性高锰酸钾溶液褪色 |
| B、分子式为C4H7ClO2,可与NaHCO3产生CO2的有机物可能结构有3种 |
C、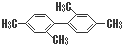 分子中至少有11个碳原子处于同一平面上 分子中至少有11个碳原子处于同一平面上 |
D、1mol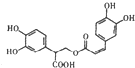 有机物 一定条件下能和7molNaOH反应 有机物 一定条件下能和7molNaOH反应 |
下列说法正确的是( )
| A、Na2O2与水的反应中,氧化剂是Na2O2,还原剂是水 |
| B、向硅酸钠溶液中滴加盐酸,有白色凝胶生成 |
| C、向AlCl3溶液中逐滴滴加氨水至过量,先出现白色沉淀后溶解 |
| D、工业上可以电解氯化镁溶液制取金属镁 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、滴入酚酞溶液显红色的溶液中:K+、Na+、Cu2+、SO42- |
| B、加入过量NaOH溶液或少量稀H2SO4时,都能产生白色沉淀的溶液:K+、Ba2+、Cl-、HCO3- |
| C、水电离产生的c(H+)=10-13 mol?L-1的溶液中:Na+、Cl-、NO3-、CH3COO- |
| D、pH=1的溶液中:Na+、NO3-、S2-、Cl- |
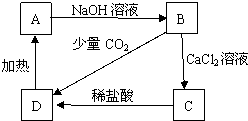 A、B、C、D均为含硅的化合物,其中B的水溶液俗称水玻璃,其相互转化关系如图所示.
A、B、C、D均为含硅的化合物,其中B的水溶液俗称水玻璃,其相互转化关系如图所示.