题目内容
7.分类是化学学习和研究中的常用手段,下列分类依据和结论都正确的是( )| A. | 浓HCl、浓H2SO4、浓HNO3均具有氧化性,都属氧化性酸 | |
| B. | 根据分散系是否有丁达尔效应将分散系分为溶液、胶体和浊液 | |
| C. | NaOH、HNO3、NaNO3在水溶液中均能电离出离子,都属离子化合物 | |
| D. | Na2O2、HCl、BaSO4在熔融状态或溶于水时均能导电,都属电解质 |
分析 A.浓HCl没有强氧化性,不是氧化性酸;
B.分散系的分类依据是根据分散系微粒直径的大小;
C.活泼金属和活泼非金属元素之间存在离子键,非金属元素之间易形成共价键,离子化合物中一定含有离子键,共价化合物中只含共价键;
D.在水溶液里或熔融状态下能导电的化合物是电解质.
解答 解:A.浓HCl没有强氧化性,不是氧化性酸,浓H2SO4、浓HNO3均具有氧化性,属氧化性酸,故A错误;
B.分散系的分类依据是根据分散系中分散质粒子直径的大小,而不是否具有丁达尔现象,故B错误;
C.HNO3只含非金属元素,属于共价化合物,故C错误;
D.Na2O2、HCl、BaSO4在熔融状态或溶于水时均能导电,都属电解质,故D正确.
故选D.
点评 本题考查物质的分类,题目难度不大,注意物质的分类的依据,侧重于基础知识的考查.

练习册系列答案
相关题目
17.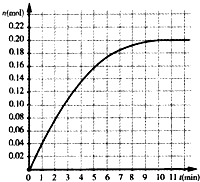 恒温条件下,往容积为2L的密闭容器内加入0.4mol的N2和1.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g),反应中NH3物质的量变化情况如图:下列说法不合理的是( )
恒温条件下,往容积为2L的密闭容器内加入0.4mol的N2和1.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g),反应中NH3物质的量变化情况如图:下列说法不合理的是( )
 恒温条件下,往容积为2L的密闭容器内加入0.4mol的N2和1.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g),反应中NH3物质的量变化情况如图:下列说法不合理的是( )
恒温条件下,往容积为2L的密闭容器内加入0.4mol的N2和1.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g),反应中NH3物质的量变化情况如图:下列说法不合理的是( )| A. | 其它条件不变,若改用5L容器达到平衡需要的时间将大于10min | |
| B. | N2平衡转化率为25% | |
| C. | 平衡时气体总压强为开始时的90% | |
| D. | 反应前10min反应速率v(H2)=0.01mol?L-1?min-1 |
2.隐形眼镜越来越受到年青人的喜爱,在使用隐形眼镜时,常用的护理药水中含有过氧化氢(H2O2).下列有关过氧化氢的说法中正确的是( )
| A. | 过氧化氢是由氢气和氧气组成的 | |
| B. | 它是由2个氢元素和2个氧元素组成的 | |
| C. | 过氧化氢在二氧化锰作用下能生成水和氧气,该反应为复分解反应 | |
| D. | 每个过氧化氢分子中含有2个氢原子和2个氧原子 |
19.NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 16g CH4与18g NH4+所含的质子数均为10NA | |
| B. | 将15.6g Na2O2投入到足量水中,反应后溶液中的氧原子数为0.4NA | |
| C. | 在1L 0.1 mol•L-1的碳酸钠溶液中,阴离子总数一定大于0.lNA | |
| D. | 2molNO和1 mol O2混合,所得气体的分子数为2NA |
16.有机物M的分子式为C6 H10O4,且1mol M与足量NaHCO3溶液反应会生成2mol气体,则M的结构(不包括立体异构)可能有( )
| A. | 9种 | B. | 10种 | C. | 11种 | D. | 12种 |
17.下列有关性质的比较,不能用元素周期律解释的是( )
| A. | 热稳定性:Na2CO3>NaHCO3 | B. | 非金属性:Cl>Br | ||
| C. | 碱性:NaOH>Mg(OH)2 | D. | 酸性:H2SO4>H3PO4 |
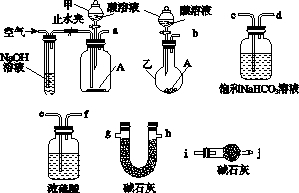 碱式碳酸盐A可用作胃药,其组成可表示为Al2Mg6(OH)x(CO3)y•zH2O.某校化学兴趣小组欲测定其化学式,实验设计如下:
碱式碳酸盐A可用作胃药,其组成可表示为Al2Mg6(OH)x(CO3)y•zH2O.某校化学兴趣小组欲测定其化学式,实验设计如下:
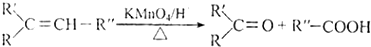
 .
.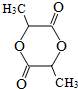 .
. .
. ,A与等物质的量的Br2进行加成反应的产物共有3种(不考虑立体异构).
,A与等物质的量的Br2进行加成反应的产物共有3种(不考虑立体异构).