题目内容
20.下列关于原电池的叙述正确的是( )| A. | 原电池中电子流出的一极是正极 | |
| B. | 原电池是将化学能转变为电能的装置 | |
| C. | 构成原电池的正极和负极必须是两种不同的金属 | |
| D. | 原电池放电时,电流的方向是从负极到正极 |
分析 原电池中电流由正极流向负极,电子流出的一极是负极,负极发生氧化反应,电解质溶液中的阴离子向负极移动;电子流进的一极是正极,正极发生还原反应,电解质溶液中的阳离子向正极移动,以此解答该题.
解答 解:A.电子流出的为负极,发生氧化反应,故A错误;
B.原电池是将化学能转变为电能的装置,故B正确;
C.构成原电池的正极和负极可以有一极是非金属导体,故C错误;
D.原电池工作时,原电池中电流由正极经导线流向负极,故D错误.
故选B.
点评 本题考查了原电池的反应原理的应用,为高频考点,侧重于学生的分析能力,注意把握电子流向、电极判断,题目难度不大.

练习册系列答案
 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
10.一定条件下,下列各组物质混合后(必要时可加热),两种反应物有可能恰好反应完全的是( )
| A. | 盐酸、MnO2 | B. | 铜片、浓硫酸 | C. | 大理石、硫酸 | D. | 银与硝酸 |
11.X、Y、Z、R是短周期主族元素,X原子最外层电子数是次外层的两倍,Y元素在地壳中的含量最多,Z元素的化合物的焰色反应呈黄色,R原子的核外电子数是X原子与Z原子的核外电子数之和.下列叙述正确的是( )
| A. | 原子半径的大小顺序:r(X)>r(Y)>r(Z)>r(R) | |
| B. | 含有Y、Z、R三种元素的化合物最多只有2种 | |
| C. | 元素R和Y形成的化合物RY2是一种高效安全灭菌消毒剂 | |
| D. | Y与Z能形成Z2Y和Z2Y2两种不同的化合物,它们的晶体类型相同 |
8.为了防止FeCl2溶液变质,可向溶液中加入( )
| A. | 铁粉 | B. | 铜粉 | C. | HCl溶液 | D. | 硝酸溶液 |
15.下列电池不属于化学电池的是( )
| A. | 一次电池 | B. | 二次电池 | C. | 燃料电池 | D. | 太阳能电池 |
5.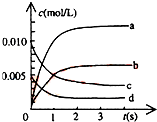 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
(1)800℃,反应达到平衡时,NO的物质的量的浓度是0.0035mol/L;
(2)图中表示NO2的浓度变化曲线是b.用O2表示从0~2s内该反应的平均速率v=0.0015mol•L-1•s-1.
(3)能说明该反应已达到平衡状态的是be.
a、v (NO2)=2v (O2)
b、容器内压强保持不变
c、v逆(NO)=v正(O2)
d、容器内混合气体的密度保持不变
e、该容器内颜色保持不变.
 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)图中表示NO2的浓度变化曲线是b.用O2表示从0~2s内该反应的平均速率v=0.0015mol•L-1•s-1.
(3)能说明该反应已达到平衡状态的是be.
a、v (NO2)=2v (O2)
b、容器内压强保持不变
c、v逆(NO)=v正(O2)
d、容器内混合气体的密度保持不变
e、该容器内颜色保持不变.
9.医学上,科学家们设计以Pt和Zn为电极材料的电池,植入人体内作为心脏病患者的心脏起搏器的能源,它依靠人体内体液中存在的一定浓度的溶解的O2、H+、Zn2+进行工作.下列叙述正确的是( )
| A. | Pt为负极,Zn为正极 | |
| B. | Zn为负极,Pt为正极 | |
| C. | 负极反应式为Zn-2e-═Zn2+,正极反应式为2H++2e-═H2↑ | |
| D. | 负极反应式为Zn-2e-═Zn2+,正极反应式为O2+2H2O+4e-═4OH- |
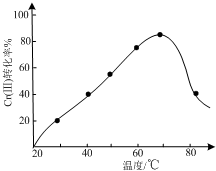 工业含铬废水的处理原理是将Cr2O72-转化为Cr3+,再将Cr3+转化为Cr(OH)3沉淀.利用硫酸工业废气中的SO2处理含铬废水,既充分利用资源、以废治废,还能节约生产成本.
工业含铬废水的处理原理是将Cr2O72-转化为Cr3+,再将Cr3+转化为Cr(OH)3沉淀.利用硫酸工业废气中的SO2处理含铬废水,既充分利用资源、以废治废,还能节约生产成本.