题目内容
 多晶硅是太阳能光伏产业的重要原料.
多晶硅是太阳能光伏产业的重要原料.(1)由石英砂可制取粗硅,其相关反应的热化学方程式如下:
SiO2(s)+C(s)=SiO(g)+CO(g)△H=a KJ?mol-1
2SiO(g)=Si(s)+SiO2(s)△H=b KJ?mol-1
①反应SiO2(s)+2C(s)=Si(s)+2CO(g)的△H=
②SiO是反应过程中的中间产物.隔绝空气时,SiO与NaOH溶液反应(产物之一是硅酸钠)的化学方程式是
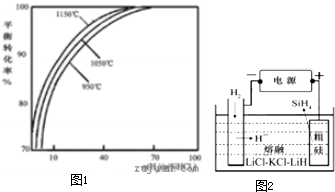
(2)粗硅提纯常见方法之一是先将粗硅与HCl制得SiHCl3,经提纯后再用H2还原:SiHCl3(g)+H2(g)?Si(s)+3HCl(g)不同温度及不同n(H2)/n(SiHCl3)时,反应物X的平衡转化率关系如图1;
①X是
②上述反应的平衡常数K(1150℃)
(3)SiH4(硅烷)法生产高纯多晶硅是非常优异的方法.
①用粗硅作原料,熔盐电解法制取硅烷原理如图2,电解时阳极的电极反应式为
②硅基太阳电池需用N、Si两种元素组成的化合物Y作钝化材料,它可由SiH4与NH3混合气体进行气相沉积得到,已知Y中Si的质量分数为60%,Y的化学式为
考点:用盖斯定律进行有关反应热的计算,硅和二氧化硅
专题:化学反应中的能量变化,碳族元素
分析:(1)①利用盖斯定律分析,不管化学反应是一步或分几步完成,其反应热是不变的;依据热化学方程式和盖斯定律构造目标热化学方程式计算反应热;
②产物之一是硅酸钠,根据质量守恒定律,化学反应前后元素的种类和原子的个数不变书写方程式;
(2)①根据图象可知:横坐标表示氢气的量增多;
②温度越高,SiHCl3的转化率高,即反应进行的程度大;
(3)①电解池中的阳极上发生失电子的氧化反应,单质硅失电子后和H-结合生成SiH4;
②Si的质量分数为60%,氧的质量分数为40%,据此确定化学式;
②产物之一是硅酸钠,根据质量守恒定律,化学反应前后元素的种类和原子的个数不变书写方程式;
(2)①根据图象可知:横坐标表示氢气的量增多;
②温度越高,SiHCl3的转化率高,即反应进行的程度大;
(3)①电解池中的阳极上发生失电子的氧化反应,单质硅失电子后和H-结合生成SiH4;
②Si的质量分数为60%,氧的质量分数为40%,据此确定化学式;
解答:
解:(1)①Ⅰ、SiO2(s)+C(s)=SiO(g)+CO(g)△H=a KJ?mol-1
Ⅱ、2SiO(g)=Si(s)+SiO2(s)△H=b KJ?mol-1
由盖斯定律可知,Ⅰ×2+Ⅱ得SiO2(s)+2C(s)=Si(s)+2CO(g),故△H=(2a+b)KJ?mol-1,
故答案为:2a+b;
②SiO与NaOH溶液反应,反应物为:SiO、NaOH,产物为Na2SiO3,根据质量守恒定律,氢氧化钠前系数为2,根据氢原子守恒产物为氢气,所以化学反应方程式为:SiO+2NaOH=Na2SiO3+H2↑,
故答案为:SiO+2NaOH=Na2SiO3+H2↑;
(2)①两种反应物,增加其中一种,另一种物质的转化率增大,自身的转化率反而减小,横坐标表示氢气的量增多,所以纵坐标表示的转化率提高应为SiHCl3,
故答案为:SiHCl3;
②当
一定时,温度越高,SiHCl3的转化率高,即反应进行的程度大,所以高温时的化学平衡常数大,则该反应的平衡常数随温度升高而增大,即K(1150℃)>K(950℃);
故答案为:>;
(3)①此题类似于电解精炼铜的原理,用粗铜作为阳极,从图示知,H-移向阳极生成SiH4,电极反应式为Si+4H--4e-=SiH4↑,
故答案为:Si+4H--4e-=SiH4↑;
②n(Si):n(N)=
:
=3:4,化学式为Si3N4,
故答案为:Si3N4.
Ⅱ、2SiO(g)=Si(s)+SiO2(s)△H=b KJ?mol-1
由盖斯定律可知,Ⅰ×2+Ⅱ得SiO2(s)+2C(s)=Si(s)+2CO(g),故△H=(2a+b)KJ?mol-1,
故答案为:2a+b;
②SiO与NaOH溶液反应,反应物为:SiO、NaOH,产物为Na2SiO3,根据质量守恒定律,氢氧化钠前系数为2,根据氢原子守恒产物为氢气,所以化学反应方程式为:SiO+2NaOH=Na2SiO3+H2↑,
故答案为:SiO+2NaOH=Na2SiO3+H2↑;
(2)①两种反应物,增加其中一种,另一种物质的转化率增大,自身的转化率反而减小,横坐标表示氢气的量增多,所以纵坐标表示的转化率提高应为SiHCl3,
故答案为:SiHCl3;
②当
| n(H2) |
| n(SiHCl3) |
故答案为:>;
(3)①此题类似于电解精炼铜的原理,用粗铜作为阳极,从图示知,H-移向阳极生成SiH4,电极反应式为Si+4H--4e-=SiH4↑,
故答案为:Si+4H--4e-=SiH4↑;
②n(Si):n(N)=
| 60% |
| 28 |
| 40% |
| 14 |
故答案为:Si3N4.
点评:本题考查硅及其化合物的性质,注意盖斯定律的应用,读懂图象、理顺平衡常数与转化率间的关系、注意电化学电极反应式的书写是解题的关键,题目难度中等.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
在一定温度下的定容密闭容器中,当物质的下列物理量不再发生变化时,不能表明该反应A(s)+2B(g)?C(g)+D(g)已达到平衡状态的是( )
| A、混合气体的密度 |
| B、混合气体的总物质的量 |
| C、混合气体的平均相对分子质量 |
| D、体系的温度不变 |

 为了制取纯净干燥的气体A,可用如图所示装置,生成A的速度可通过滴入液体B的速度控制,已知A是一种无色、无味、不能使酸碱指示剂变色、不会在空气中燃烧的气体,但能使带火星的木条复燃.
为了制取纯净干燥的气体A,可用如图所示装置,生成A的速度可通过滴入液体B的速度控制,已知A是一种无色、无味、不能使酸碱指示剂变色、不会在空气中燃烧的气体,但能使带火星的木条复燃.