题目内容
2.利用下列实验装置能完成相应实验的是( )| A. |  装置可干燥、收集并吸收多余的NH3 | |
| B. |  装置除去CO2中含有的少量HCl | |
| C. |  装置可以制备大量的乙炔气体 | |
| D. |  装置不添加任何仪器即可检查气密性 |
分析 A.氨气的密度比空气密度小,利用向下排空气法收集;
B.二者均与碳酸钠溶液反应;
C.反应生成的氢氧化钙易堵塞启普发生器中的瓶颈;
D.利用液柱法可检验气密性.
解答 解:A.氨气的密度比空气密度小,利用向下排空气法收集,则收集气体装置不合理,故A错误;
B.二者均与碳酸钠溶液反应,不能除杂,试剂瓶中应为碳酸氢钠,故B错误;
C.反应生成的氢氧化钙易堵塞启普发生器中的瓶颈,则制备乙炔不能使用启普发生器,故C错误;
D.推动活塞,导管内形成一段液柱,一段时间内高度不变,则该装置不添加任何仪器即可检查气密性,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握实验基本操作、实验技能及实验装置的作用为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.以下验证元素的金属性、非金属性强弱的实验,所用物品不合理的是( )
| A. | 比较钾、钠:Na、K、H2O | |
| B. | 比较镁、铝:MgCl2溶液、AlCl3溶液、NaOH溶液 | |
| C. | 比较硫、氯:Na2S溶液、NaCl溶液、pH试纸 | |
| D. | 比较溴、碘:溴水、KI淀粉试纸 |
10.化学用语准确的是( )
| A. | 铁触煤 | B. | 氨盐 | C. | 硬脂酸 | D. | 活性碳 |
17.类比推断是学习化学的一种重要方法,推断正确的是( )
| A. | 电解熔融NaCl制取Na,故电解熔融MgCl2也能制取Mg | |
| B. | Fe与CuSO4溶液反应置换出Cu,故Na也能从CuSO4溶液中置换出Cu | |
| C. | 通常元素的价态越高对应物质的氧化性越强,故HClO4的氧化性强于HClO | |
| D. | CO2和Na2O2反应生成Na2CO3和O2,故SO2和Na2O2反应生成Na2SO3和O2 |
7.某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应:A(g)+xB(g)?2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间的变化关系如图所示.下列说法中正确的是( )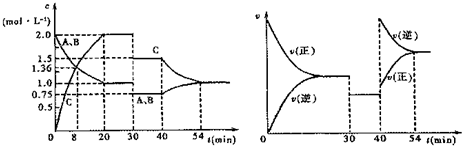

| A. | 反应方程式中的x=1 | |
| B. | 该反应为放热反应 | |
| C. | 30 min时改变的条件是加入催化剂 | |
| D. | 前30 min内A的反应速率为0.05 mol/(L•min) |
11.观察如图装置,下列说法正确的是( )
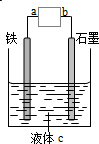

| A. | a、b接电流表,该装置为原电池 | |
| B. | a、b接直流电源,该装置为电解池 | |
| C. | a、b接直流电源,铁可能不易被腐蚀 | |
| D. | a、b接电流表或接直流电源,铁都可能是负极 |
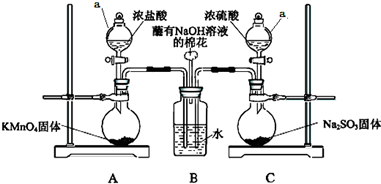 某实验小组欲探究SO2和Cl2能否发生反应,设计如下图所示的实验装置进行实验.
某实验小组欲探究SO2和Cl2能否发生反应,设计如下图所示的实验装置进行实验.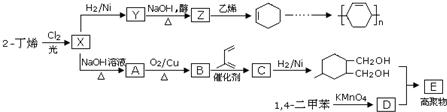
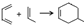 .
.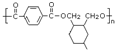 ;甲是A的一种同分异构体,其能实现转化:
;甲是A的一种同分异构体,其能实现转化: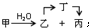 ,甲的名称为乙酸乙酯;
,甲的名称为乙酸乙酯;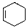 可以合成
可以合成 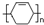 .按合成路线的顺序,涉及反应的反应类型有:加成、消去、加聚.
.按合成路线的顺序,涉及反应的反应类型有:加成、消去、加聚.