题目内容
6.①将Cu片放入稀硫酸中,铜片未溶解.但是如果此时加入一定量的H2O2,则可以看到溶液变蓝,相关离子方程式为Cu+H2O2+2H+=Cu2++2H2O②在一定温度下,向15g蒸馏水加入无水硫酸铜粉末,充分搅拌并过滤,得到一定质量的蓝色晶体和8.4g滤液,若此温度下无水硫酸铜的溶解度为40g,则原先加入的无水硫酸铜的物质的量为多少?(要求有必要的推导过程)
分析 ①在酸性条件下,双氧水氧化Cu,生成Cu2+,溶液变蓝;
②此温度下无水硫酸铜的溶解度为40g,可知140g硫酸铜溶液中有40g硫酸铜;则8.4g滤液含有硫酸铜为2.4g,有6g水;原本有水15g,则有15g-6g=9g水进入硫酸铜晶体中,可以计算出晶体中硫酸铜为16g,共含有硫酸铜为2.4g+16g=18.4g,进而求其物质的量.
解答 解:①在酸性条件下,双氧水氧化Cu,生成Cu2+,溶液变蓝,离子方程式为:Cu+H2O2+2H+=Cu2++2H2O;
故答案为:Cu+H2O2+2H+=Cu2++2H2O;
②此温度下无水硫酸铜的溶解度为40g,可知140g硫酸铜溶液中有40g硫酸铜;则8.4g滤液含有硫酸铜为:$\frac{40g}{140g}=\frac{m}{8.4g}$,m=2.4g,有6g水;原本有水15g,则有15g-6g=9g水进入硫酸铜晶体中,可以计算出晶体中硫酸铜为16g,共含有硫酸铜为2.4g+16g=18.4g,其物质的量为0.115mol;
故答案为:0.115mol.
点评 本题以氧化还原反应为载体考查离子方程式的书写,溶解度的相关计算,注意硫酸铜分为两部分,一部分存在于蓝色晶体中,一部分存在于滤液中.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.如果将20mL 12mol•L-1的浓盐酸与足量KMnO4充分反应,实际能收集到的氯气在标准状况下的体积将( )
| A. | ≥1.68L | B. | >1.68L | C. | ≤1.68L | D. | <1.68L |
17.下列溶液一定是碱性的是( )
| A. | 溶液中含有OH- | B. | 滴加甲基橙后溶液显红色 | ||
| C. | 溶液中c(OH-)>c(H+) | D. | 滴加甲基橙后溶液显黄色 |
1.某温度下,浓度都是1mol•L-1的两种气体X2和Y2,在密闭容器中反应生成气体Z,经过t min后,测得各物质的浓度分别为c(X2)=0.4mol•L-1,c(Y2)=0.6mol•L-1,c(Z)=0.4mol•L-1,则该反应的化学方程式可表示为( )
| A. | 2X2+3Y2?2X2Y3 | B. | 3X2+2Y2?2X3Y2 | C. | X2+2Y22?XY2 | D. | 2X2+Y2?2X2Y |
11.将0.2mol•L-1HCOOH溶液加水稀释,下列说法正确的是( )
| A. | 溶液中c(H+)和c(OH-)都减小 | B. | 溶液中c(H+)增大 | ||
| C. | 醋酸电离平衡向左移动 | D. | 溶液的pH增大 |
18.下面是有关弱酸的电离平衡常数
结合数据,分析下列有关说法,其中错误的是( )
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7,K2=5.6×10-11 |
| A. | 1mol•L-1的溶液中,pH(HCN)>pH(H2CO3)>pH(CH3COOH) | |
| B. | 升高温度,HCN溶液中HCN的电离平衡正向移动,电离平衡常数增大 | |
| C. | 0.2mol/L醋酸溶液与0.1mol/L醋酸溶液中c(H+)之比小于2:1 | |
| D. | 饱和H2CO3溶液中c(H+)与c(CO32-)的比值小于2:1 |
15.下列说法正确的是( )
| A. | 工业上用二氧化硅在高温下与焦炭反应,生成单质硅和二氧化碳的原理,制取粗硅 | |
| B. | 手指不慎被玻璃划伤流血,可向伤口上涂FeCl3溶液,是因为FeCl3溶液可杀菌消毒 | |
| C. | 2014年山东莱芜共出现284天雾霾天气,对煤进行液化和气化等物理变化的处理,可减少雾霾天气的发生 | |
| D. | 白酒放置一定时间香味更浓,是因为白酒中乙醇与少量的有机酸反应生成有香味的酯 |
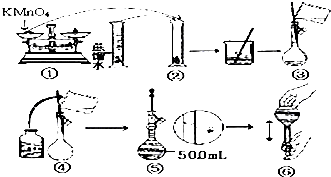 人体血液里Ca2+离子的浓度一般采用g/cm3来表示.抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得一种弱酸草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度.某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度:
人体血液里Ca2+离子的浓度一般采用g/cm3来表示.抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得一种弱酸草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度.某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度: