题目内容
钯/碳高效绿色催化Suzuki 交叉偶联反应是近年来有机合成的热点之一,如
反应①:
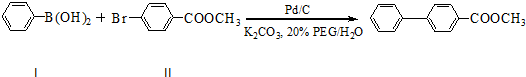
化合物Ⅱ可由化合物Ⅲ合成:

(1)化合物Ⅱ的分子式为 ,含有的官能团名称为 .
(2)化合物Ⅳ的结构简式为 .
(3)化合物Ⅵ与新制Cu(OH)2悬浊液反应的化学方程式为 (注明条件).
(4)化合物Ⅴ的一种同分异构体Ⅷ遇FeCl3溶液显紫色,核磁共振氢谱峰面积之比为2:2:2:1,则化合物Ⅷ的结构简式为 .写出化合物Ⅷ与足量NaOH水溶液反应的化学方程式为(注明条件) .
反应①:
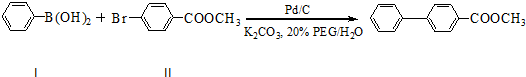
化合物Ⅱ可由化合物Ⅲ合成:

(1)化合物Ⅱ的分子式为
(2)化合物Ⅳ的结构简式为
(3)化合物Ⅵ与新制Cu(OH)2悬浊液反应的化学方程式为
(4)化合物Ⅴ的一种同分异构体Ⅷ遇FeCl3溶液显紫色,核磁共振氢谱峰面积之比为2:2:2:1,则化合物Ⅷ的结构简式为
考点:有机物的推断,有机物的合成
专题:有机物的化学性质及推断
分析:(1)根据化合物Ⅱ的结构简式书写分子式,判断有机物的官能团;
(2)由转化关系可知,化合物Ⅲ中甲基上1个H原子被Cl原子取代生成化合物Ⅳ,化合物Ⅳ为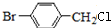 ,化合物Ⅳ发生水解反应生成化合物Ⅴ(
,化合物Ⅳ发生水解反应生成化合物Ⅴ(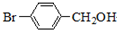 ),化合物Ⅴ连续氧化生成化合物Ⅶ,则化合物Ⅵ为
),化合物Ⅴ连续氧化生成化合物Ⅶ,则化合物Ⅵ为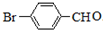 ,Ⅶ为
,Ⅶ为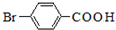 ,化合物Ⅶ与甲醇发生酯化反应生成化合物Ⅱ;
,化合物Ⅶ与甲醇发生酯化反应生成化合物Ⅱ;
(3) 与新制氢氧化铜反应生成
与新制氢氧化铜反应生成 、氧化亚铜、水;
、氧化亚铜、水;
(4)化合物Ⅴ( )一种同分异构体Ⅷ遇FeCl3溶液显紫色,含有酚羟基,核磁共振氢谱峰面积之比为2:2:2:1,则化合物Ⅷ的结构简式为
)一种同分异构体Ⅷ遇FeCl3溶液显紫色,含有酚羟基,核磁共振氢谱峰面积之比为2:2:2:1,则化合物Ⅷ的结构简式为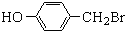 .
.
(2)由转化关系可知,化合物Ⅲ中甲基上1个H原子被Cl原子取代生成化合物Ⅳ,化合物Ⅳ为
 ,化合物Ⅳ发生水解反应生成化合物Ⅴ(
,化合物Ⅳ发生水解反应生成化合物Ⅴ( ),化合物Ⅴ连续氧化生成化合物Ⅶ,则化合物Ⅵ为
),化合物Ⅴ连续氧化生成化合物Ⅶ,则化合物Ⅵ为 ,Ⅶ为
,Ⅶ为 ,化合物Ⅶ与甲醇发生酯化反应生成化合物Ⅱ;
,化合物Ⅶ与甲醇发生酯化反应生成化合物Ⅱ;(3)
 与新制氢氧化铜反应生成
与新制氢氧化铜反应生成 、氧化亚铜、水;
、氧化亚铜、水;(4)化合物Ⅴ(
 )一种同分异构体Ⅷ遇FeCl3溶液显紫色,含有酚羟基,核磁共振氢谱峰面积之比为2:2:2:1,则化合物Ⅷ的结构简式为
)一种同分异构体Ⅷ遇FeCl3溶液显紫色,含有酚羟基,核磁共振氢谱峰面积之比为2:2:2:1,则化合物Ⅷ的结构简式为 .
.解答:
解:(1)根据化合物Ⅱ的结构简式,可知其分子式为C8H7O2Br,含有的官能团有:酯基、溴原子,
故答案为:C8H7O2Br;酯基、溴原子;
(2)由转化关系可知,化合物Ⅲ中甲基上1个H原子被Cl原子取代生成化合物Ⅳ,化合物Ⅳ为 ,化合物Ⅳ发生水解反应生成化合物Ⅴ(
,化合物Ⅳ发生水解反应生成化合物Ⅴ( ),化合物Ⅴ连续氧化生成化合物Ⅶ,则化合物Ⅵ为
),化合物Ⅴ连续氧化生成化合物Ⅶ,则化合物Ⅵ为 ,Ⅶ为
,Ⅶ为 ,化合物Ⅶ与甲醇发生酯化反应生成化合物Ⅱ,故答案为:
,化合物Ⅶ与甲醇发生酯化反应生成化合物Ⅱ,故答案为: ;
;
(3) 与新制氢氧化铜反应生成
与新制氢氧化铜反应生成 、氧化亚铜、水,反应方程式为:
、氧化亚铜、水,反应方程式为: ,
,
故答案为: ;
;
(4)化合物Ⅴ( )一种同分异构体Ⅷ遇FeCl3溶液显紫色,含有酚羟基,核磁共振氢谱峰面积之比为2:2:2:1,则化合物Ⅷ的结构简式为
)一种同分异构体Ⅷ遇FeCl3溶液显紫色,含有酚羟基,核磁共振氢谱峰面积之比为2:2:2:1,则化合物Ⅷ的结构简式为 ,化合物Ⅷ与足量NaOH水溶液反应的化学方程式为:
,化合物Ⅷ与足量NaOH水溶液反应的化学方程式为: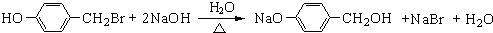 ,
,
故答案为: ;
;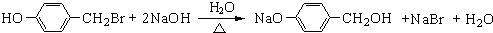 .
.
故答案为:C8H7O2Br;酯基、溴原子;
(2)由转化关系可知,化合物Ⅲ中甲基上1个H原子被Cl原子取代生成化合物Ⅳ,化合物Ⅳ为
 ,化合物Ⅳ发生水解反应生成化合物Ⅴ(
,化合物Ⅳ发生水解反应生成化合物Ⅴ( ),化合物Ⅴ连续氧化生成化合物Ⅶ,则化合物Ⅵ为
),化合物Ⅴ连续氧化生成化合物Ⅶ,则化合物Ⅵ为 ,Ⅶ为
,Ⅶ为 ,化合物Ⅶ与甲醇发生酯化反应生成化合物Ⅱ,故答案为:
,化合物Ⅶ与甲醇发生酯化反应生成化合物Ⅱ,故答案为: ;
;(3)
 与新制氢氧化铜反应生成
与新制氢氧化铜反应生成 、氧化亚铜、水,反应方程式为:
、氧化亚铜、水,反应方程式为: ,
,故答案为:
 ;
;(4)化合物Ⅴ(
 )一种同分异构体Ⅷ遇FeCl3溶液显紫色,含有酚羟基,核磁共振氢谱峰面积之比为2:2:2:1,则化合物Ⅷ的结构简式为
)一种同分异构体Ⅷ遇FeCl3溶液显紫色,含有酚羟基,核磁共振氢谱峰面积之比为2:2:2:1,则化合物Ⅷ的结构简式为 ,化合物Ⅷ与足量NaOH水溶液反应的化学方程式为:
,化合物Ⅷ与足量NaOH水溶液反应的化学方程式为: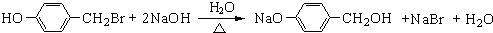 ,
,故答案为:
 ;
;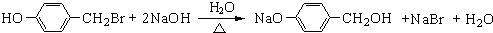 .
.
点评:本题考查有机物的推断,注意根据转化关系中有机物的结构与反应条件进行推断,较好的考查学生的阅读能力,对知识的迁移运用能力,需要学生熟练掌握官能团的性质与转化,难度中等.

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案
相关题目
下列有关化学事实或现象解释正确的是( )
| A、加热煮沸MgCO3悬浊液,最终得到Mg(OH)2沉淀,说明Ksp(MgCO3)<Ksp[Mg(OH)2] |
| B、胆矾晶体投入浓硫酸中变成白色固体是化学变化 |
| C、电解AlCl3水溶液,阴极周围出现白色胶状沉淀,说明Al(OH)3胶体粒子带正电荷 |
| D、气体甲通入溶液乙,溶液乙颜色褪去,说明气体甲一定有漂白性 |
在一定条件下,下列反应及其化学平衡常数数值如下:以下说法正确的是( )
2NO(g)?N2(g)+O2(g) K1=1×103
2H2(g)+O2(g)?2H2O(g) K2=2×109
2CO2(g)?2CO(g)+O2(g) K3=4×10-9.
2NO(g)?N2(g)+O2(g) K1=1×103
2H2(g)+O2(g)?2H2O(g) K2=2×109
2CO2(g)?2CO(g)+O2(g) K3=4×10-9.
| A、此条件下,可认为NO分解产生O2的反应完全 |
| B、此条件下,2H2O(g)=2H2 (g)+O2(g),此时平衡常数的数值约为5×10-10 |
| C、此条件下,NO、H2O、CO2三种物质分解放出O2的倾向由大到小的顺序为H2O>NO>CO2 |
| D、以上说法都不正确 |
下列叙述正确的是( )
| A、加入BaCl2溶液有白色沉淀产生,再加盐酸,沉淀不消失,原溶液一定有SO42- |
| B、滴入KMnO4酸性溶液,紫红色褪去,证明CH2=CHCH2CHO中一定有碳碳不饱和键 |
| C、能使湿润的红色石蕊试纸变蓝,该气体的水溶液一定显碱性 |
| D、加入稀盐酸,产生无色并能使澄清石灰水变浑浊的气体,原溶液一定有CO32-或SO32- |
常温下,某一元弱酸的电离平衡常数为:Ka=10-6,对于0.01mol?L-1的该酸,下列说法不正确是( )
| A、该弱酸溶液的pH=4 |
| B、加入NaOH溶液后,弱酸的电离平衡向右移动,但Ka不变 |
| C、加入等体积的0.01mol?L-1NaOH溶液后,所得的溶液的pH<7 |
| D、该弱酸的钠盐溶液一定会发生水解,常温下,其水解平衡常数Kh=10-8 |

