题目内容
15.下列电离方程式中,不正确的是( )| A. | HCl═H++Cl- | B. | NH3•H2O═NH4++OH- | ||
| C. | CaCl2=Ca2++2Cl- | D. | CH3COOH?CH3COO-+H+ |
分析 强电解质完全电离,用等号,弱电解质部分电离,用可逆号,据此解答.
解答 解:A.氯化氢为强电解质,完全电离,电离方程式:HCl═H++Cl-,故A正确;
B.一水合氨为弱电解质,部分电离,电离方程式:NH3•H2O?NH4++OH-,故B错误;
C.氯化钙为强电解质,完全电离,电离方程式:CaCl2=Ca2++2Cl-,故C正确;
D.醋酸为弱电解质,部分电离,电离方程式:CH3COOH?CH3COO-+H+,故D正确;
故选:B.
点评 本题考查了电解质电离方程式的书写,明确电解质强弱及电离方式是解题关键,注意电离方程式遵循原子个数、电荷数守恒规律.

练习册系列答案
相关题目
5.在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)?2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如表:
下列说法正确的是( )
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A. | 0~2 min的平均速率v(Z)=2.0×10-3 mol•L-1•min-1 | |
| B. | 其他条件不变,降低温度,反应达到新平衡时v(正)>v(逆) | |
| C. | 该温度下此反应的平衡常数K=144 | |
| D. | 其他条件不变,再充入0.2 mol Z,平衡时X的体积分数不变 |
3.X、Y、Z三种金属及其化合物间可发生如下反应:
Y+ZCl2═Z+YCl2 X+ZCl2═Z+XCl2
Y+2HCl═YCl2+H2↑ X+HCl→不反应
则X、Y、Z三种金属活动性由强至弱的顺序是( )
Y+ZCl2═Z+YCl2 X+ZCl2═Z+XCl2
Y+2HCl═YCl2+H2↑ X+HCl→不反应
则X、Y、Z三种金属活动性由强至弱的顺序是( )
| A. | Z>X>Y | B. | X>Y>Z | C. | Y>X>Z | D. | Y>Z>X |
10.下列不属于我国“城市空气质量日报”报道内容的是( )
| A. | SO2 | B. | CO2 | C. | PM2.5 | D. | 空气质量等级 |
20.若用NA表示阿伏加德罗常数的值,则下列说法错误的是( )
| A. | NA个18O2和NA个NO的质量比为16:15 | |
| B. | 标准状况下1molCO和CO2的混合物的体积约占22.4L | |
| C. | 24gMg在足量空气中完全燃烧失去2NA个电子 | |
| D. | 常温下,18gH2O含有的电子数为10NA |
7.下列说法正确的是( )
| A. | 可用澄清石灰水鉴别Na2CO3和NaHCO3溶液 | |
| B. | 浓硫酸具有吸水性,可做干燥剂,但不能干燥NH3 | |
| C. | 钠保存在煤油中,若长期放置在空气中,最终变为NaHCO3 | |
| D. | 镁着火后可以用CO2来灭火 |
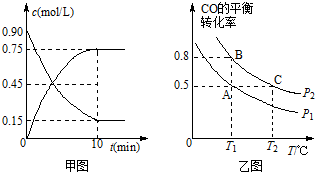
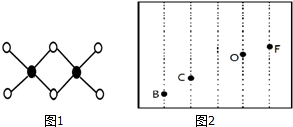 硼及其化合物在工业上有许多用途.工业上以铁硼矿为原料制备硼酸,铁硼矿含有Mg、Fe、Ca、Al、B、O等多种元素,它的主要成分为Mg2B2O5•H2O和Fe3O4.
硼及其化合物在工业上有许多用途.工业上以铁硼矿为原料制备硼酸,铁硼矿含有Mg、Fe、Ca、Al、B、O等多种元素,它的主要成分为Mg2B2O5•H2O和Fe3O4.