题目内容
根据反应8NH3+3Cl2=6NH4Cl+N2,回答下列问题:
(1)该反应中氧化剂是 ,被氧化的是 元素.
(2)该反应中参加氧化还原的氧化剂与还原剂的物质的量之比为 .
(3)用双线桥法标出电子转移的方向与数目 .
(1)该反应中氧化剂是
(2)该反应中参加氧化还原的氧化剂与还原剂的物质的量之比为
(3)用双线桥法标出电子转移的方向与数目
考点:氧化还原反应
专题:氧化还原反应专题
分析:反应8NH3+3Cl2═6NH4Cl+N2,N元素的化合价升高,Cl元素的化合价降低,该反应中转移6e-,以此来解答.
解答:
解:(1)反应中Cl元素的化合价降低,则Cl2为氧化剂,N元素的化合价升高,失去电子被氧化,故答案为:Cl2;N;
(2)由反应可知,3mol氧化剂与2mol还原剂转移电子相等,则氧化剂与还原剂的物质的量之比为3:2,故答案为:3:2.
(3)用双线桥标出电子转移的方向和数目可为 ,故答案为:
,故答案为: .
.
(2)由反应可知,3mol氧化剂与2mol还原剂转移电子相等,则氧化剂与还原剂的物质的量之比为3:2,故答案为:3:2.
(3)用双线桥标出电子转移的方向和数目可为
 ,故答案为:
,故答案为: .
.
点评:本题考查氧化还原反应,为高考高频考点,把握发生的化学反应及反应中元素的化合价变化为解答的关键,侧重基本概念和转移电子的考查,题目难度不大.

练习册系列答案
相关题目
下列化学式能准确表示物质分子组成的是( )
| A、NH4Cl |
| B、C6H5NO2 |
| C、SiO2 |
| D、Cu |
下列物质属于混合物的是( )
| A、冰水混合物 |
| B、盐酸 |
| C、纯醋酸 |
| D、CuSO4?5H2O |
下列有关物质的分类正确的是( )
| A、混合物:空气、矿泉水、水银 |
| B、碱:Ba(OH)2、纯碱、NH3?H2O |
| C、盐:石灰石、氯化铵、NaHSO4 |
| D、酸性氧化物:CO2、CO、SO2 |
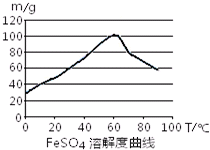 铁盐、亚铁盐在工农业生产、生活、污水处理等方面有着极其广泛的应用.用铁屑与硫酸反应制备FeSO4
铁盐、亚铁盐在工农业生产、生活、污水处理等方面有着极其广泛的应用.用铁屑与硫酸反应制备FeSO4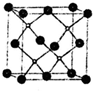 2010上海世博上,零排放、太阳能、绿色光源等成为高科技亮点.
2010上海世博上,零排放、太阳能、绿色光源等成为高科技亮点.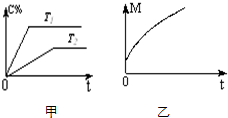 在密闭容器中投入一定量的A和B发生反应:m A(g)+n B(g)?p C(g)+q D(g).
在密闭容器中投入一定量的A和B发生反应:m A(g)+n B(g)?p C(g)+q D(g).