题目内容
下列离子或分子在溶液中能大量共存,通入SO2后仍能大量共存的一组是( )
| A、Na+、Mg2+、Cl-、ClO- |
| B、NH3?H2O、SO32-、K+、Na+ |
| C、Fe2+、Na+、K+、NO3- |
| D、K+、Ca2+、Br-、Cl- |
考点:离子共存问题
专题:
分析:A.通入二氧化硫后,次氯酸根离子能够氧化二氧化硫;
B.二氧化硫能够与一水合氨、亚硫酸根离子反应;
C.二氧化硫溶于水生成亚硫酸,溶液显示酸性,硝酸根离子在酸性条件下能够氧化亚铁离子;
D.K+、Ca2+、Br-、Cl-离子之间不发生反应,通入二氧化硫后也不发生反应.
B.二氧化硫能够与一水合氨、亚硫酸根离子反应;
C.二氧化硫溶于水生成亚硫酸,溶液显示酸性,硝酸根离子在酸性条件下能够氧化亚铁离子;
D.K+、Ca2+、Br-、Cl-离子之间不发生反应,通入二氧化硫后也不发生反应.
解答:
解:A.通入SO2后,SO2与ClO-之间发生氧化还原反应,在溶液中不能大量共存,故A错误;
B.通入SO2后,SO2与NH3?H2O、SO32-之间反应,在溶液中不能大量共存,故B错误;
C.通入SO2后,SO2与与水反应生成亚硫酸,溶液显示酸性,NO3-在酸性条件下能够氧化Fe2+,在溶液中不能大量共存,故C错误;
D.K+、Ca2+、Br-、Cl-离子之间生反应,通入SO2后也不发生反应,在溶液中能够大量共存,故D正确;
故选D.
B.通入SO2后,SO2与NH3?H2O、SO32-之间反应,在溶液中不能大量共存,故B错误;
C.通入SO2后,SO2与与水反应生成亚硫酸,溶液显示酸性,NO3-在酸性条件下能够氧化Fe2+,在溶液中不能大量共存,故C错误;
D.K+、Ca2+、Br-、Cl-离子之间生反应,通入SO2后也不发生反应,在溶液中能够大量共存,故D正确;
故选D.
点评:本题考查离子共存的判断,为高考中的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;本题中通入二氧化硫后,需要明确二氧化硫具有还原性,其溶液显示酸性.

练习册系列答案
相关题目
有一真空瓶质量为m1,该瓶充入二氧化碳气体后质量为m2.在相同状况下,若改为充入某气体A时,总质量为m3.则A的相对分子质量是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列叙述不正确的是( )
| A、在实验室里硅酸钠溶液存放在带橡胶塞的试剂瓶中 |
| B、提倡人们购物时不用塑料袋,是为了防止白色污染 |
| C、氟利昂(CCl2F2)因破坏大气臭氧层而导致“温室效应” |
| D、为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术 |
下列表示20Ca的基态原子的核外电子排布不正确的是( )
A、 |
B、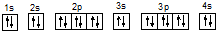 |
| C、1s22s22p63s23p64s2 |
| D、1s22s22p63s23p63d2 |
下列实验操作中错误的是( )
| A、蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 |
| B、蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶支管口处,且冷凝水方向应当由下往上 |
| C、分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D、提取碘水中的碘单质时,应选择有机萃取剂,且萃取剂与水不互溶 |
 化学反应原理在生活和生产中有着广泛的应用.利用“化学蒸气转移法”制备TaS2晶
化学反应原理在生活和生产中有着广泛的应用.利用“化学蒸气转移法”制备TaS2晶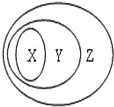 用如图表示的一些物质或概念间的从属关系中不正确的是( )
用如图表示的一些物质或概念间的从属关系中不正确的是( )