题目内容
 CaC2可用于固氮:CaC2+N2
CaC2可用于固氮:CaC2+N2
| ||
(1)写出与Ca在同一周期且最外层电子数相同、内层电子排满的基态原子的电子排布式
(2)C、N、O三种元素的第一电离能由小到大的顺序是
(3)NH3中N原子的杂化方式为;根据价层电子对互斥理论推测CO32-的空间构型为
(4)CaCN2中阴离子为CN22-,与CN22-互为等电子体的分子有
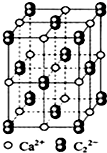
(5)CaC2晶体的晶胞结构与NaCl晶体的相似(如图所示),其晶胞的边长为a×10-7cm,则该晶体的密度为
考点:原子核外电子排布,元素电离能、电负性的含义及应用,判断简单分子或离子的构型,“等电子原理”的应用,晶胞的计算
专题:
分析:(1)Ca位于第四周期、最外层电子数为2,最外层电子数为2、内层排满电子的第四周期元素原子是Zn,电子排布式为1s22s22p63s23p63d104s2或[Ar]3d104s2;
(2)同周期元素从左向右,第一电离能总体趋势增大,但IIA和VA反常,第一电离能:C<O<N;
(3)NH3中N形成3个δ键,还有1对孤对电子,N杂化类型为sp3;CO32-中C价层电子对数=
=3,C与3个O成键,空间构型为平面三角形;
(4)等电子体原子数相同、价电子数相同.C2-与O原子数相等,所以与CN22-互为等电子体的分子有N2O,N2与CO互为等电子体,与N2O互为等电子体的分子有CO2、BeCl2等;CaCN2与水生成NH3,同时生成CaCO3;CaCN2 +3H2O=CaCO3+2NH3↑;
(5)CaC2晶体的晶胞结构与NaCl晶体的相似,该晶胞中含有Ca为12×
+1=4;一个晶胞中含有4个CaC2;则该晶体的密度ρ=
=
g/cm3=
g/cm3.
(2)同周期元素从左向右,第一电离能总体趋势增大,但IIA和VA反常,第一电离能:C<O<N;
(3)NH3中N形成3个δ键,还有1对孤对电子,N杂化类型为sp3;CO32-中C价层电子对数=
| 4+0×3+2 |
| 2 |
(4)等电子体原子数相同、价电子数相同.C2-与O原子数相等,所以与CN22-互为等电子体的分子有N2O,N2与CO互为等电子体,与N2O互为等电子体的分子有CO2、BeCl2等;CaCN2与水生成NH3,同时生成CaCO3;CaCN2 +3H2O=CaCO3+2NH3↑;
(5)CaC2晶体的晶胞结构与NaCl晶体的相似,该晶胞中含有Ca为12×
| 1 |
| 4 |
| m |
| V |
| 4×84 |
| (a×10-7)3 |
| 336 |
| a3×10-21 |
解答:
解:(1)Ca位于第四周期、最外层电子数为2,最外层电子数为2、内层排满电子的第四周期元素原子是Zn,电子排布式为1s22s22p63s23p63d104s2或[Ar]3d104s2;故答案为:1s22s22p63s23p63d104s2或[Ar]3d104s2;
(2)同周期元素从左向右,第一电离能总体趋势增大,但IIA和VA反常,第一电离能:C<O<N;δ
故答案为:C<O<N;
(3)NH3中N形成3个δ键,还有1对孤对电子,N杂化类型为sp3;CO32-中C价层电子对数=
=3,C与3个O成键,空间构型为平面三角形;故答案为:平面三角形;
(4)等电子体原子数相同、价电子数相同.C2-与O原子数相等,所以与CN22-互为等电子体的分子有N2O,N2与CO互为等电子体,与N2O互为等电子体的分子有CO2、BeCl2等;CaCN2与水生成NH3,同时生成CaCO3;CaCN2 +3H2O=CaCO3+2NH3↑;
故答案为:N2O;CaCN2 +3H2O=CaCO3+2NH3↑;
(5)CaC2晶体的晶胞结构与NaCl晶体的相似,该晶胞中含有Ca为12×
+1=4;一个晶胞中含有4个CaC2;则该晶体的密度ρ=
=
g/cm3=
g/cm3;故答案为:
g/cm3.
(2)同周期元素从左向右,第一电离能总体趋势增大,但IIA和VA反常,第一电离能:C<O<N;δ
故答案为:C<O<N;
(3)NH3中N形成3个δ键,还有1对孤对电子,N杂化类型为sp3;CO32-中C价层电子对数=
| 4+0×3+2 |
| 2 |
(4)等电子体原子数相同、价电子数相同.C2-与O原子数相等,所以与CN22-互为等电子体的分子有N2O,N2与CO互为等电子体,与N2O互为等电子体的分子有CO2、BeCl2等;CaCN2与水生成NH3,同时生成CaCO3;CaCN2 +3H2O=CaCO3+2NH3↑;
故答案为:N2O;CaCN2 +3H2O=CaCO3+2NH3↑;
(5)CaC2晶体的晶胞结构与NaCl晶体的相似,该晶胞中含有Ca为12×
| 1 |
| 4 |
| m |
| V |
| 4×84 |
| (a×10-7)3 |
| 336 |
| a3×10-21 |
| 336 |
| a3×10-21 |
点评:本题考查核外电子排布式 第一电离能 中心原子杂化类型 离子空间构型 等电子体 化学方程式的书写,难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
A、相同条件下,结合质子的能力:OH->AlO2->CO32->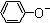 >HCO3->CH3COO- >HCO3->CH3COO- |
B、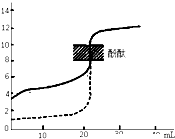 如图表示用0.1mol/LNaOH溶液分别滴定相同物质的量浓度和相同体积的盐酸和醋酸,其中实线表示的是滴定盐酸的曲线 |
| C、一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率,平衡常数保持不变 |
| D、恒容密闭容器中进行的反应A(g)?B(g)+C(g),在其它条件不变情况下,再充入一定量的A气体,A的转化率将增大 |
1.52g铜镁合金完全溶解于50mL 63%的浓硝酸(硝酸密度为1.40g/mL)中,得到标况下NO2和N2O4 的混合气体1120mL.向反应后的溶液中加入1.0mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀,下列说法不正确的是 ( )
| A、该合金中nCu:nMg=2:1 |
| B、合金完全溶解时,溶液中C(H+)=8mol/L(忽略反应前后溶液体积变化) |
| C、NO2和N2O4的混合气体中,NO2的体积分数是80% |
| D、得到2.54g沉淀时,加入NaOH溶液的体积是600mL. |
在含有Cu(NO3)2、Fe(NO3)3、AgNO3各0.1mol的混合溶液中加入铁粉,经充分反应后铁粉完全溶解,过滤、洗涤、干燥得固体产物12.4g,则溶解的铁粉的质量是( )
| A、5.6 g |
| B、7 g |
| C、2.8 g |
| D、8.4 g |
下列有关实验的叙述正确的是( )
| A、蒸发皿可用来研磨块状固体物质 |
| B、锥形瓶作为反应容器时一定不能加热 |
| C、分液漏斗不宜盛装碱性溶液 |
| D、可用湿润的蓝色石蕊试纸检测氨气 |
下列有关实验原理或操作正确的是( )
A、 分离沸点相差较大的互溶液体混合物 |
B、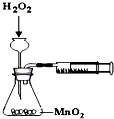 测定化学反应速率 |
C、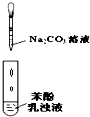 比较苯酚、碳酸的酸性强弱 |
D、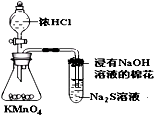 比较KMnO4、Cl2、S的氧化性 |