题目内容
8分)Cu2S和稀HNO3反应生成Cu(NO3)2、H2SO4、NO和H2O,试解答下列各题
(1)配平上述反应方程式并标出电子转移的方向和总数
(2)当产生0.1mol NO时,转移电子总数为 ,被还原的物质为 mol,共耗HNO3 mol。
(3)被1mol Cu2S中+1价亚铜离子还原的HNO3的物质的量是 mol
【答案】
 (1)3Cu2S+22HNO3(稀)═6Cu(NO3)2+10NO↑+3H2SO4+8H2O
(1)3Cu2S+22HNO3(稀)═6Cu(NO3)2+10NO↑+3H2SO4+8H2O
|
|||
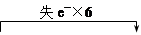 |

 或:3Cu2S+22HNO3(稀)═6Cu(NO3)2+10NO↑+3H2SO4+8H2O
或:3Cu2S+22HNO3(稀)═6Cu(NO3)2+10NO↑+3H2SO4+8H2O
 |
(2)
0.3×6.02×1023或1.806×1023 ; 0.1;0.22 ;(3)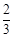 ;
;
【解析】

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目