题目内容
某校研究小组的同学通过实验探究了CuO对氯酸钾分解的催化作用,并与MnO2相比较,研究其催化能力.部分实验数据如下表:
回答下列问题:
(1)上表中a= g,b= g,c= g.
(2)实验①的目的是 .
(3)本实验中为了比较CuO和MnO2对氯酸钾分解的催化能力,还需测量的数据是: .
(4)实验中为了更准确地说明CuO和MnO2对氯酸钾分解的催化能力,还应保持反应的温度相同,如果该实验是在你校的实验室进行,你将如何操作以保证反应温度相同 .
(5)从反应残留物中回收催化剂,并称量其质量,目的是 .
| 实验编号 | m(KClO3)/g | m(MnO2)/g | m(CuO)/g | 回收催化剂质量/g |
| ① | 0.6000 | -- | -- | -- |
| ② | a | 0.2000 | -- | 0.1950 |
| ③ | b | -- | c | 0.1900 |
(1)上表中a=
(2)实验①的目的是
(3)本实验中为了比较CuO和MnO2对氯酸钾分解的催化能力,还需测量的数据是:
(4)实验中为了更准确地说明CuO和MnO2对氯酸钾分解的催化能力,还应保持反应的温度相同,如果该实验是在你校的实验室进行,你将如何操作以保证反应温度相同
(5)从反应残留物中回收催化剂,并称量其质量,目的是
考点:探究浓度、催化剂对化学平衡的影响
专题:实验题
分析:本实验的目的是比较两种氧化物的催化性能,因此前提条件是所取KClO3和两种氧化物的质量分别相等,通过相同时间内放出O2的量来判断两种氧化物催化性能的高低.(1)为了对比合理,在反应开始加入的反应物和催化剂的质量都应该相等;
(2)实验①未加催化剂,就是为了对比一下实验②③加入催化剂的效果如何;
(3)催化剂可以加快反应速率,反应速率的大小可以通过测量生成氧气的快慢程度判断;
(4)保证温度相同,可以用大小相似的火焰,沙浴加热也能保证受热均匀;
(5)催化剂在反应前后的质量和化学性质是不变的,测量一下看是否符合催化剂的这一性质.
(2)实验①未加催化剂,就是为了对比一下实验②③加入催化剂的效果如何;
(3)催化剂可以加快反应速率,反应速率的大小可以通过测量生成氧气的快慢程度判断;
(4)保证温度相同,可以用大小相似的火焰,沙浴加热也能保证受热均匀;
(5)催化剂在反应前后的质量和化学性质是不变的,测量一下看是否符合催化剂的这一性质.
解答:
解:(1)为了对比合理,加入的KClO3质量和催化剂的质量应该相等,在实验②③中氯酸钾的质量要等于实验①中氯酸钾的质量,实验③CuO的质量也应该等于实验②中二氧化锰的质量;
故答案为:0.6000;0.6000;0.2000;
(2)实验①未加催化剂,测量生成氧气的速率,可以作为实验②、③的对照,看MnO2、CuO对KClO3的分解能否起到加速的作用,也就是看能否起到催化剂的作用;
故答案为:作为实验②、③的对照,看MnO2、CuO对KClO3的分解能否起催化作用;
(3)催化剂可以加快反应速率,为了验证CuO和MnO2对氯酸钾的分解是否起到催化效果,需要测量生成氧气的速率,可以通过测量相同时间内放出O2的量或放出等量的O2所需的时间来判断化学反应速率;
故答案为:相同时间内放出O2的量或放出等量的O2所需的时间;
(4)保持反应的温度相同,可以用大小相似的火焰,沙浴加热也能保证受热均匀;
故答案为:用火焰大小相似的酒精灯加热相同时间或用控温电炉加热相同时间或水浴加热相同时间等;
(5)催化剂在反应前后的质量和化学性质是不变的,测量一下看是否符合催化剂的这一性质,可以观察反应前后CuO、MnO2的质量是否发生变化,以进一步说明它们在反应中是否起催化作用.
故答案为:观察反应前后CuO、MnO2的质量是否发生变化,以进一步说明它们在反应中是否起催化作用.
故答案为:0.6000;0.6000;0.2000;
(2)实验①未加催化剂,测量生成氧气的速率,可以作为实验②、③的对照,看MnO2、CuO对KClO3的分解能否起到加速的作用,也就是看能否起到催化剂的作用;
故答案为:作为实验②、③的对照,看MnO2、CuO对KClO3的分解能否起催化作用;
(3)催化剂可以加快反应速率,为了验证CuO和MnO2对氯酸钾的分解是否起到催化效果,需要测量生成氧气的速率,可以通过测量相同时间内放出O2的量或放出等量的O2所需的时间来判断化学反应速率;
故答案为:相同时间内放出O2的量或放出等量的O2所需的时间;
(4)保持反应的温度相同,可以用大小相似的火焰,沙浴加热也能保证受热均匀;
故答案为:用火焰大小相似的酒精灯加热相同时间或用控温电炉加热相同时间或水浴加热相同时间等;
(5)催化剂在反应前后的质量和化学性质是不变的,测量一下看是否符合催化剂的这一性质,可以观察反应前后CuO、MnO2的质量是否发生变化,以进一步说明它们在反应中是否起催化作用.
故答案为:观察反应前后CuO、MnO2的质量是否发生变化,以进一步说明它们在反应中是否起催化作用.
点评:本题属于正向思维能力的考查,只要弄清实验目的和实验原理不难解决,本实验的目的是比较两种氧化物的催化性能,因此前提条件是所取KClO3和两种氧化物的质量分别相等,通过相同时间内放出O2的量的来判断催化性能的高低.要牢牢抓住催化剂在反应前后的质量和化学性质是不变的这一性质来求解.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
一定温度下,在2L的密闭容器中发生如下反应:A(s)+2B(g)?xC(g)△H<0,B、C的物质的量随时间变化的关系如图1,达平衡后在t1、t2、t3、t4时都只改变了一种条件,逆反应速率随时间变化的关系如图2
下列有关说法正确的是( )
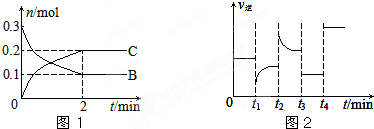
下列有关说法正确的是( )

| A、x=2,反应开始2 min内,v(B)=0.1 mol/(L?min) |
| B、t3时可能是减小压强,平衡不移动;t4时可能是使用催化剂,c(B)不变 |
| C、t2时改变的条件可能是增大c(C),B的转化率增大 |
| D、t1时改变的条件可能是降温,A(s)的质量增加 |
