题目内容
创造新的有机物是有机化学的重要课题,发现并选择利用有机反应,把反应物转化为目标生成物是制取有机物的关键.已知几种常见的有机物之间的转化关系如下图所示.

(1)有机物A的结构简式是 .乙酸乙酯的结构简式是 .
(2)反应②的反应类型是 .反应④的反应类型是 .
(3)下列化合物中,不属于烃类的是 (填字母).
a.乙炔 b.乙烯 c.氯乙烯
(4)在发生反应④时,有机物A分子断裂的化学键是 (填“C-H”、“C-O”或“O-H”)键,该反应的反应条件是 、 .
(5)写出金属钠与足量乙酸溶液反应的离子方程式,并用单线桥标出电子转移的方向和数目: .

(1)有机物A的结构简式是
(2)反应②的反应类型是
(3)下列化合物中,不属于烃类的是
a.乙炔 b.乙烯 c.氯乙烯
(4)在发生反应④时,有机物A分子断裂的化学键是
(5)写出金属钠与足量乙酸溶液反应的离子方程式,并用单线桥标出电子转移的方向和数目:
考点:有机物的合成
专题:有机物的化学性质及推断
分析:在题中各物质转化关系中,反应①为乙炔与氢气加成生成乙烯(CH2=CH2),反应②为乙烯与水加成生成A为CH3CH2OH,反应③为乙醇发生氧化反应生成乙醛(CH3CHO),反应④为乙醇与乙酸发生酯化反应生成乙酸乙酯(CH3COOCH2CH3),反应⑤为乙炔与氯化氢加成生成氯乙烯,反应⑥为氯乙烯发生加聚反应生成聚氯乙烯( ),钠与足量乙酸溶液反应生成乙酸钠和氢气,每摩尔钠反应转移1mol电子,据此答题;
),钠与足量乙酸溶液反应生成乙酸钠和氢气,每摩尔钠反应转移1mol电子,据此答题;
 ),钠与足量乙酸溶液反应生成乙酸钠和氢气,每摩尔钠反应转移1mol电子,据此答题;
),钠与足量乙酸溶液反应生成乙酸钠和氢气,每摩尔钠反应转移1mol电子,据此答题;解答:
解:在题中各物质转化关系中,反应①为乙炔与氢气加成生成乙烯(CH2=CH2),反应②为乙烯与水加成生成A为CH3CH2OH,反应③为乙醇发生氧化反应生成乙醛(CH3CHO),反应④为乙醇与乙酸发生酯化反应生成乙酸乙酯(CH3COOCH2CH3),反应⑤为乙炔与氯化氢加成生成氯乙烯,反应⑥为氯乙烯发生加聚反应生成聚氯乙烯( ),
),
(1)根据上面的分析可知,有机物A的结构简式是CH3CH2OH,乙酸乙酯的结构简式是CH3COOCH2CH3,
故答案为:CH3CH2OH;CH3COOCH2CH3;
(2)反应②的反应类型是 加成反应,反应④的反应类型是取代(酯化)反应,
故答案为:加成反应;取代(酯化)反应;
(3)烃是由碳、氢两种元素组成的有机物,所以氯乙烯不属于烃,
故选c;
(4)在酯化反应时,羧脱羟基醇脱氢,所以在发生反应④时,有机物A分子断裂的化学键是 O-H键,该反应的反应条件是浓硫酸、加热,
故答案为:O-H;浓硫酸、加热;
(5)金属钠与足量乙酸溶液反应的离子方程式并用单线桥标出电子转移的方向和数目为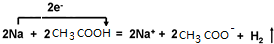 ,
,
故答案为: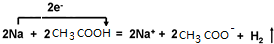 ;
;
 ),
),(1)根据上面的分析可知,有机物A的结构简式是CH3CH2OH,乙酸乙酯的结构简式是CH3COOCH2CH3,
故答案为:CH3CH2OH;CH3COOCH2CH3;
(2)反应②的反应类型是 加成反应,反应④的反应类型是取代(酯化)反应,
故答案为:加成反应;取代(酯化)反应;
(3)烃是由碳、氢两种元素组成的有机物,所以氯乙烯不属于烃,
故选c;
(4)在酯化反应时,羧脱羟基醇脱氢,所以在发生反应④时,有机物A分子断裂的化学键是 O-H键,该反应的反应条件是浓硫酸、加热,
故答案为:O-H;浓硫酸、加热;
(5)金属钠与足量乙酸溶液反应的离子方程式并用单线桥标出电子转移的方向和数目为
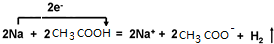 ,
,故答案为:
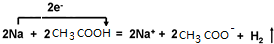 ;
;
点评:本题考查有机物的结构和性质,涉及方程式的书写、结构简式的书写等知识点,明确物质的结构和性质是解本题关键,熟练掌握有机物之间的转化,题目难度不大.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
在强酸性溶液中能大量共存的无色透明离子组是( )
| A、K+、Na+、NO3-、CO32- |
| B、Mg2+、Na+、Cl-、SO42- |
| C、K+、Na+、Br-、Cu2+ |
| D、Na+、Ba2+、NO3-、HCO3- |
下列化合物的沸点比较,前者低于后者的是( )
| A、乙醇与氯乙烷 |
B、 邻羟基苯甲酸与 邻羟基苯甲酸与 对羟基苯甲酸 对羟基苯甲酸 |
C、 对羟基苯甲醛与 对羟基苯甲醛与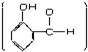 邻羟基苯甲醛 邻羟基苯甲醛 |
| D、H2O与H2Te |
同温同压下在两个容积相同的容器中,一个盛有HCl气体,另一个盛有H2和Cl2的混合气体.两容器内的气体一定具有相同的是( )
| A、摩尔质量 | B、密度 |
| C、质量 | D、分子数 |
设NA表示阿伏伽德罗常数,下列说法正确的是( )
| A、标准状况下,22.4LSO3含有NA个分子 |
| B、标准状况下,22.4LCO2与CO的混合气体含NA个分子 |
| C、lmolNa2O2与足量CO2反应转移的电子数为NA |
| D、常温下NA个H2分子的质量约为2g,它所占的体积约为22.4L |
将0.56g铁粉加入到25mL 2mol?L-1的氯化铁溶液中,充分反应后其结果是( )
| A、铁有剩余,溶液呈浅绿色,Cl-浓度保持不变 |
| B、往溶液中滴无色KSCN溶液,溶液呈浅绿色 |
| C、Fe2+和Fe3+的物质的量之比为6:1 |
| D、氧化产物与还原产物的物质的量之比为1:2 |
下列有关物质性质和应用的说法正确的是( )
| A、碳酸钠受热易分解,可用于生产食品发酵粉 |
| B、次氯酸钠具有强氧化性,可用于配制消毒液 |
| C、二氧化硅不与强酸反应,可用石英玻璃容器盛放氢氟酸 |
| D、二氧化硫有漂白、杀菌性能,可在食品生产中大量使用 |
