题目内容
16.下列离子方程式正确的是( )| A. | 铜片插入FeCl3溶液中:Cu+2Fe3+═Cu2++2 Fe2+ | |
| B. | 氯化铝溶液中加入过量的氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| C. | 烧碱溶液中加铝片:2Al+2OH-+2H2O═2 AlO2-+3H2↑ | |
| D. | 铁粉与稀盐酸的反应:2Fe+6H+═2Fe3++3H2↑ |
分析 A.反应生成氯化亚铁和氯化铜;
B.反应生成氢氧化铝和氯化铵;
C.反应生成偏铝酸钠和氢气;
D.反应生成氯化亚铁和氢气.
解答 解:A.铜片插入FeCl3溶液中的离子反应为Cu+2Fe3+═Cu2++2Fe2+,遵循电子、电荷守恒,故A正确;
B.氯化铝溶液中加入过量的氨水的离子反应为Al3++3NH3•H2O═Al(OH)3↓+3NH4+,故B错误;
C.烧碱溶液中加铝片的离子反应为2Al+2OH-+2H2O═2AlO2-+3H2↑,故C正确;
D.铁粉与稀盐酸的反应的离子反应为Fe+2H+═Fe2++H2↑,故D错误;
故选AC.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
相关题目
6.聚合氯化铝是一种新型净水剂,其中铝的总浓度(用AlT表示)包括三类:主要为Al3+的单体形态铝总浓度(用Ala表示);主要为[AlO4Al12(OH)24(H2O)12]7+的中等聚合形态铝总浓度(用Alb表示)和Al(OH)3胶体形态铝总浓度(用A1c表示).
(1)一定条件下,向1.0mol/LAlCl3溶液中加入0.6mol/L的NaOH溶液,可制得Alb含量约为86%的聚合氯化铝溶液.写出生成[AlO4Al12(OH)24(H2O)12]7+的离子方程式:13Al3++32OH-+8H2O=[AlO4Al12(OH)24(H2O)12]7+.
(2)用膜蒸馏(简称MD)浓缩技术将聚合氯化铝溶液进行浓缩,实验过程中不同浓度聚合氯化铝中铝形态分布(百分数)如表:
①在一定温度下,AlT越大,pH越小(填“越大”、“越小”或“不变”).
②如将AlT=2.520mol•L-1的聚合氯化铝溶液加水稀释,则稀释过程中主要发生反应的离子方程式:Al3++3H2O?Al(OH)3(胶体)+3H+.
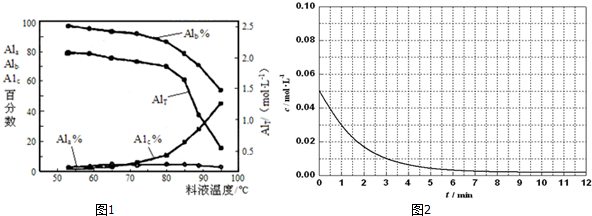
③膜蒸馏料液温度对铝聚合形态百分数及铝的总浓度的影响如图1.当T>80℃时,AlT显著下降的原因是温度升高,水解程度加大,产生氢氧化铝沉淀.
(3)真空碳热还原一氧化法可实现由铝土矿制备金属铝,相关反应的热化学方程式如下:
①Al2O3(s)+AlCl3(g)+3C(s)=3AlCl(g)+3CO(g)△H1=a kJ•mol-1
②3AlCl(g)=2Al(l)+AlCl3(g)△H2=b kJ•mol-1
则反应Al2O3(s)+3C(s)=2Al(l)+3CO(g)△H=(a+b)kJ•mol-1(用含a、b的代数式表示).反应①常压下在1900℃的高温下才能进行,说明△H>0(填“>”“=”或“<”).
(4)物质中的铝元素可以通过将铝元素转化成Al3+,然后在水溶液中用铝试剂(NH4)3C19H11O3(COO)3(商品名为“阿罗明拿)测定,在弱酸性溶液中,Al3+可以用铝试剂反应,生成玫瑰红色的物质.随着该反应的进行,溶液的颜色不断变化,分析溶液颜色与反应物(或生成物)浓度的关系(即比色分析),可以确定该化学反应的速率.用于比色分析的仪器是C.
A.pH计 B.元素分析仪 C.分光光度计 D.原子吸收光谱仪
(5)已知Al3++4X?2[(Al${\;}_{\frac{1}{2}}$X2)1.5+],X表示显色剂,Al${\;}_{\frac{1}{2}}$X21.5+表示有色物质,通过比色分析得到25℃时Al3+浓度随时间的变化关系如图2所示,请在同一图中绘出Al${\;}_{\frac{1}{2}}$X21.5+浓度随时间的变化曲线.
(1)一定条件下,向1.0mol/LAlCl3溶液中加入0.6mol/L的NaOH溶液,可制得Alb含量约为86%的聚合氯化铝溶液.写出生成[AlO4Al12(OH)24(H2O)12]7+的离子方程式:13Al3++32OH-+8H2O=[AlO4Al12(OH)24(H2O)12]7+.
(2)用膜蒸馏(简称MD)浓缩技术将聚合氯化铝溶液进行浓缩,实验过程中不同浓度聚合氯化铝中铝形态分布(百分数)如表:
| AlT/(mol•L-1) | Ala/% | Alb/% | A1c/% |
| 0.208 | 1.4 | 86.6 | 12.0 |
| 0.489 | 2.3 | 86.2 | 11.5 |
| 0.884 | 2.3 | 88.1 | 9.6 |
| 1.613 | 3.1 | 87.0 | 9.9 |
| 2.520 | 4.5 | 88.2 | 7.3 |
②如将AlT=2.520mol•L-1的聚合氯化铝溶液加水稀释,则稀释过程中主要发生反应的离子方程式:Al3++3H2O?Al(OH)3(胶体)+3H+.
③膜蒸馏料液温度对铝聚合形态百分数及铝的总浓度的影响如图1.当T>80℃时,AlT显著下降的原因是温度升高,水解程度加大,产生氢氧化铝沉淀.

(3)真空碳热还原一氧化法可实现由铝土矿制备金属铝,相关反应的热化学方程式如下:
①Al2O3(s)+AlCl3(g)+3C(s)=3AlCl(g)+3CO(g)△H1=a kJ•mol-1
②3AlCl(g)=2Al(l)+AlCl3(g)△H2=b kJ•mol-1
则反应Al2O3(s)+3C(s)=2Al(l)+3CO(g)△H=(a+b)kJ•mol-1(用含a、b的代数式表示).反应①常压下在1900℃的高温下才能进行,说明△H>0(填“>”“=”或“<”).
(4)物质中的铝元素可以通过将铝元素转化成Al3+,然后在水溶液中用铝试剂(NH4)3C19H11O3(COO)3(商品名为“阿罗明拿)测定,在弱酸性溶液中,Al3+可以用铝试剂反应,生成玫瑰红色的物质.随着该反应的进行,溶液的颜色不断变化,分析溶液颜色与反应物(或生成物)浓度的关系(即比色分析),可以确定该化学反应的速率.用于比色分析的仪器是C.
A.pH计 B.元素分析仪 C.分光光度计 D.原子吸收光谱仪
(5)已知Al3++4X?2[(Al${\;}_{\frac{1}{2}}$X2)1.5+],X表示显色剂,Al${\;}_{\frac{1}{2}}$X21.5+表示有色物质,通过比色分析得到25℃时Al3+浓度随时间的变化关系如图2所示,请在同一图中绘出Al${\;}_{\frac{1}{2}}$X21.5+浓度随时间的变化曲线.
7.现用的燃料大多来自化石,但化石燃料极有可能在几百年内全部被人类耗尽.因此,燃料的充分燃烧是节约能源的重要手段.下列措施中能使燃料充分燃烧的是( )
| A. | 燃烧大块固体燃料 | B. | 把液体燃料雾化后燃烧 | ||
| C. | 燃烧时空气应不足量 | D. | 燃烧时空气应越多越好 |
11.下列说法正确的是( )
| A. | 氢氧燃料电池可将热能直接转变为电能 | |
| B. | 铁制品上镀铜时,镀件为阳极,铜盐为电镀液 | |
| C. | 镀锌铁皮的镀层损坏后,铁更容易腐蚀 | |
| D. | 铅蓄电池充电时Pb极与外电源的负极相连 |
8.已知短周期主族元素X、Y、Z、W的原子序数依次增大,X元素原子的最外层电子数是内层电子数的3倍,Y与X能形成两种化合物,Z所在的周期序数与族序数相同,W与X同主族,下列说法正确的是( )
| A. | Y的单质能从Z的盐溶液中置换出Z | B. | 氢化物的热稳定性:X>W | ||
| C. | Y、Z两元素只能形成阳离子 | D. | 简单离子的半径大小:W>Y>Z>X |
12.工业上用难溶于水的碳酸锶(SrCO3)粉末为原料(含少量钡和铁的化合物)制备高纯六水氯化锶晶体(SrCl2•6H2O),其过程为:
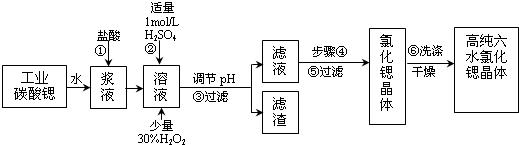
已知:Ⅰ.有关氢氧化物沉淀的pH:
Ⅱ.SrCl2•6H2O 晶体在61℃时开始失去结晶水,100℃时失去全部结晶水.
(1)操作①中碳酸锶与盐酸反应的离子方程式SrCO3+2H+=Sr2++CO2↑+H2O.
(2)在步骤②-③的过程中,将溶液的pH值由1调节至B;宜用的试剂为E.
A.1.5 B.3.7 C.9.7 D.氨水 E.氢氧化锶粉末 F.碳酸钠晶体
(3)操作②中加入H2O2发生反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O.
(4)操作③中所得滤渣的主要成分是Fe(OH)3、BaSO4 (填化学式).
(5)工业上用热风吹干六水氯化锶,适宜的温度是A.
A.50~60℃B.80~100℃C.100℃以上
(6)步骤⑥宜选用的无机洗涤剂是饱和氯化锶溶液.

已知:Ⅰ.有关氢氧化物沉淀的pH:
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 |
| 沉淀完全的pH | 3.7 | 9.7 |
(1)操作①中碳酸锶与盐酸反应的离子方程式SrCO3+2H+=Sr2++CO2↑+H2O.
(2)在步骤②-③的过程中,将溶液的pH值由1调节至B;宜用的试剂为E.
A.1.5 B.3.7 C.9.7 D.氨水 E.氢氧化锶粉末 F.碳酸钠晶体
(3)操作②中加入H2O2发生反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O.
(4)操作③中所得滤渣的主要成分是Fe(OH)3、BaSO4 (填化学式).
(5)工业上用热风吹干六水氯化锶,适宜的温度是A.
A.50~60℃B.80~100℃C.100℃以上
(6)步骤⑥宜选用的无机洗涤剂是饱和氯化锶溶液.