题目内容
CH4催化还原NOx可以消除氮氧化物的污染.例如:
①CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g);ΔH=-574 kJ/mol
②CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g);ΔH=-1160 kJ/mol
下列说法不正确的是
①CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g);ΔH=-574 kJ/mol
②CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g);ΔH=-1160 kJ/mol
下列说法不正确的是
[ ]
A.反应①②均为放热反应
B.反应①②转移的电子数相同
C.由反应①可推知:CH4(g)+4NO2(g)==4NO(g)+CO2(g)+2H2O(l) ΔH=-a kJ/mol,a<574
D.若用标准状况下4.48LCH4通过上述反应还原NO2至N2,放出的热量为173.4 kJ
B.反应①②转移的电子数相同
C.由反应①可推知:CH4(g)+4NO2(g)==4NO(g)+CO2(g)+2H2O(l) ΔH=-a kJ/mol,a<574
D.若用标准状况下4.48LCH4通过上述反应还原NO2至N2,放出的热量为173.4 kJ
C

练习册系列答案
相关题目
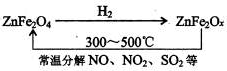

 环境保护是目前人类面临的一项重大课题.为应对燃料使用造成的环境污染,科学家构想了利用太阳能促进燃料的循环使用,其构想可用如图表示:
环境保护是目前人类面临的一项重大课题.为应对燃料使用造成的环境污染,科学家构想了利用太阳能促进燃料的循环使用,其构想可用如图表示: