题目内容
19.已知NA为阿伏伽德罗常数,下列叙述正确的是( )| A. | 标准状况下,2.24L H2O含有的分子数为0.1NA | |
| B. | 标准状况下,2.24L H2 含有的分子数为0.1mol | |
| C. | 分子数为NA 的CO和N2混合气体的体积约为22.4L,质量为28g | |
| D. | 1mol CH4分子中所含的电子总数为10 NA |
分析 A、标况下水为液态;
B、求出氢气的物质的量,然后根据分子个数N=nNA来分析;
C、气体所处的状态不明确;
D、甲烷为10电子微粒.
解答 解:A、标况下水为液态,故不能根据气体摩尔体积来计算其物质的量,故A错误;
B、标况下2.24L氢气的物质的量为0.1mol,故分子个数N=nNA=0.1NA个,故B错误;
C、气体所处的状态不明确,故体积无法计算,故C错误;
D、甲烷为10电子微粒,故1mol甲烷中含10NA个电子,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
10.基态原子的核外电子排布为4d105s1的元素应在( )
| A. | S区、第五周期、ⅠA族 | B. | ds区、第五周期、ⅠB族 | ||
| C. | d区、第四周期、ⅠB族 | D. | ds区、第五周期、ⅠA族 |
14.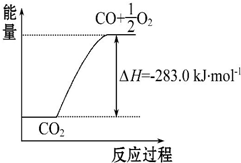 已知:①CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-283.0kJ•mol-1
已知:①CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-283.0kJ•mol-1
②H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8kJ•mol-1.
下列说法正确的是( )
 已知:①CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-283.0kJ•mol-1
已知:①CO(g)+$\frac{1}{2}$O2(g)═CO2(g)△H=-283.0kJ•mol-1②H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8kJ•mol-1.
下列说法正确的是( )
| A. | 通常状况下,氢气的燃烧热为241.8 kJ•mol-1 | |
| B. | 由①可知,1 mol CO(g)和$\frac{1}{2}$mol O2(g)反应生成1 mol CO2(g),放出283.0 kJ的热量 | |
| C. | 可用右图表示2CO2(g)═2CO(g)+O2(g)反应过程中的能量变化关系 | |
| D. | 分解1 mol H2O(g),其反应热为-241.8 KJ |
4.下列实验能获得成功的是( )
| A. | 苯与浓溴水反应制溴苯 | |
| B. | 在浓溴水中加几滴苯酚观察到白色沉淀 | |
| C. | 将乙醛滴入银氨溶液中制银镜 | |
| D. | 1mol/L CuSO4溶液2mL和0.5mol/L NaOH溶液4mL混合后加入40%乙醛溶液0.5mL,加热煮沸观察沉淀颜色 |
9.下列各组混合物中,用分液漏斗不能分离的是( )
| A. | 苯和水 | B. | 正己烷和水 | C. | 乙酸乙酯和水 | D. | 乙酸和乙醇 |
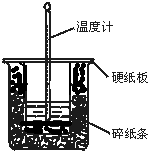 50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: