��Ŀ����
�������ƣ�CaO2��������������������ҩ�����졢��֬Ư����������������������Ϊ�������������SO2ͨ��������ƹ����ĩ�����������ɣ����������CO2��SO2��������Ƶķ�Ӧԭ����ͬ�����O2���ɣ���Ҳ���������SO2���н�ǿ�Ļ�ԭ�ԣ�CO2��ǿ��ԭ�ԣ���Ӧԭ������ͬ��O2���ɣ��ݴ��������ʵ����������жϣ�
ʵ��һ��ͨ����������IJ����жϷ����Ļ�ѧ��Ӧ��ʵ��װ�����£�
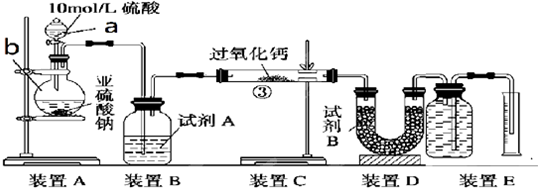
��1�����b���������� ��
��2���Լ�A����ѡ�� ���Լ�B�������� ��
��3�����װ��A�������ԵIJ��������� ��
ʵ�������һ�����Ĺ������ƹ�����ͨ������SO2��ȡ��Ӧ��Ĺ������ʵ��̽������֤������������SO2��Ӧ���ص㣮
��4��������裺
����1����Ӧ�������ֻ��Na2SO3��SO2δ������
��д����Ӧ�Ļ�ѧ����ʽ�� ��
����2����Ӧ�������ֻ�� ��SO2��ȫ������
��д����Ӧ�Ļ�ѧ����ʽ�� ��
ʵ��һ��ͨ����������IJ����жϷ����Ļ�ѧ��Ӧ��ʵ��װ�����£�

��1�����b����������
��2���Լ�A����ѡ��
��3�����װ��A�������ԵIJ���������
ʵ�������һ�����Ĺ������ƹ�����ͨ������SO2��ȡ��Ӧ��Ĺ������ʵ��̽������֤������������SO2��Ӧ���ص㣮
��4��������裺
����1����Ӧ�������ֻ��Na2SO3��SO2δ������
��д����Ӧ�Ļ�ѧ����ʽ��
����2����Ӧ�������ֻ��
��д����Ӧ�Ļ�ѧ����ʽ��
���㣺����ʵ�鷽�������
ר�⣺ʵ�������
��������1����������b�Ĺ���д�������ƣ�
��2���������ƺ�ˮ��Ӧ��װ��B���Լ�������ˮ�����������Լ�AΪŨ���װ��EΪ��ˮ���ⶨ�����������װ��D��Ҫ��ȥδ��Ӧ�Ķ������ݴ��ж��Լ�B�����ã�
��3������ʵ�����г��õļ���װ�������Եķ������
��4������Ӧ�����ֻ��Na2SO3������������������Ʒ�Ӧ�����������ƺ�������֤��SO2δ�������������Ӧ�������ֻ��Na2SO4�������������������Ӧ���������ƣ�֤��SO2��ȫ���������ݴ˽��н��
��2���������ƺ�ˮ��Ӧ��װ��B���Լ�������ˮ�����������Լ�AΪŨ���װ��EΪ��ˮ���ⶨ�����������װ��D��Ҫ��ȥδ��Ӧ�Ķ������ݴ��ж��Լ�B�����ã�
��3������ʵ�����г��õļ���װ�������Եķ������
��4������Ӧ�����ֻ��Na2SO3������������������Ʒ�Ӧ�����������ƺ�������֤��SO2δ�������������Ӧ�������ֻ��Na2SO4�������������������Ӧ���������ƣ�֤��SO2��ȫ���������ݴ˽��н��
���
�⣺��1������ͼʾװ�ÿ�֪������bΪԲ����ƿ���ʴ�Ϊ��Բ����ƿ��
��2���������ƣ�CaO2����ˮ��Ӧ��װ��A���Լ���Ҫ��ˮ�����������Լ�AΪŨ���ᣬ���ڸ��������ȥˮ������
װ��EΪ�ⶨ����������������Ҫ��ʣ��Ķ��������ȥ�������Լ�B������������δ��Ӧ��SO2��
�ʴ�Ϊ��Ũ�������δ��Ӧ��SO2��
��3�����װ��A�������ԵIJ�������Ϊ���رշ�Һ©���Ļ�������װ��B�м�����ˮ����B��ĵ��ܲ���Һ�����£��þƾ����ȷ�Һ©������ʱB��������ð����ֹͣ������ȴ��B�е����γ�ˮ���������������ã�
�ʴ�Ϊ���رշ�Һ©���Ļ�������װ��B�м�����ˮ����B��ĵ��ܲ���Һ�����£��þƾ����ȷ�Һ©������ʱB��������ð����ֹͣ������ȴ��B�е����γ�ˮ���������������ã�
��4������1����Ӧ�������ֻ��Na2SO3��SO2δ�����������������������Ӧ�����������ƺ���������Ӧ�Ļ�ѧ����ʽΪ��2Na2O2+2SO2=2Na2SO3+O2��
����������ȫ������ʱ������������������Ʒ�Ӧ���������ƣ���Ӧ�Ļ�ѧ����ʽΪ��2Na2O2+2SO2=2Na2SO4����Ӧ����ֻ��Na2SO4��
�ʴ�Ϊ��2Na2O2+2SO2=2Na2SO3+O2��Na2SO4��2Na2O2+2SO2=2Na2SO4��
��2���������ƣ�CaO2����ˮ��Ӧ��װ��A���Լ���Ҫ��ˮ�����������Լ�AΪŨ���ᣬ���ڸ��������ȥˮ������
װ��EΪ�ⶨ����������������Ҫ��ʣ��Ķ��������ȥ�������Լ�B������������δ��Ӧ��SO2��
�ʴ�Ϊ��Ũ�������δ��Ӧ��SO2��
��3�����װ��A�������ԵIJ�������Ϊ���رշ�Һ©���Ļ�������װ��B�м�����ˮ����B��ĵ��ܲ���Һ�����£��þƾ����ȷ�Һ©������ʱB��������ð����ֹͣ������ȴ��B�е����γ�ˮ���������������ã�
�ʴ�Ϊ���رշ�Һ©���Ļ�������װ��B�м�����ˮ����B��ĵ��ܲ���Һ�����£��þƾ����ȷ�Һ©������ʱB��������ð����ֹͣ������ȴ��B�е����γ�ˮ���������������ã�
��4������1����Ӧ�������ֻ��Na2SO3��SO2δ�����������������������Ӧ�����������ƺ���������Ӧ�Ļ�ѧ����ʽΪ��2Na2O2+2SO2=2Na2SO3+O2��
����������ȫ������ʱ������������������Ʒ�Ӧ���������ƣ���Ӧ�Ļ�ѧ����ʽΪ��2Na2O2+2SO2=2Na2SO4����Ӧ����ֻ��Na2SO4��
�ʴ�Ϊ��2Na2O2+2SO2=2Na2SO3+O2��Na2SO4��2Na2O2+2SO2=2Na2SO4��
���������⿼��������ʵ�鷽������ƣ��漰������������Ӧ�ú�ʵ����֤����Ŀ�Ѷ��еȣ����ؼ��Ƕ��������Ϣ�����ݷ�Ӧ���������жϣ�������������ѧ���ķ�����������������ѧʵ��������

��ϰ��ϵ�д�
�����Ŀ
����˵����ȷ���ǣ�������
| A��SO2 ��CO2�ķ������幹�;�Ϊֱ���� |
| B��H2O��NH3 �е�����ԭ���ӻ���ʽ��ͬ |
| C��SiO2�ļ�������CO2�ļ���������SiO2���۵��CO2�� |
| D�����Ǿ��й������εĹ��嶼�Ǿ��� |
��֪����Cl2ͨ������KOH��Һ�������п�����KC1��KClO��KC1O3����
��ֵ���¶ȸߵ��йأ���n��KOH��=amolʱ�������й�˵��������ǣ�������
| c(Cl-) |
| c(ClO-) |
A����ij�¶��£���Ӧ��C��Cl-����C��ClO-��=11������Һ��C��ClO-����C��ClO3-��=
| ||||
B���μӷ�Ӧ�����������ʵ�������
| ||||
C���ı��¶ȣ���Ӧ��ת�Ƶ��ӵ����ʵ���n�ķ�Χ��
| ||||
D���ı��¶ȣ�������KC1O3��������۲���Ϊ
|
235 92 |
235 92 |
A��
| ||||
B��
| ||||
C��
| ||||
D��
|
��֪25��ʱ�й����ʵĵ���ƽ�ⳣ��
��������������ǣ�������
| ��ѧʽ | CH3COOH | HClO | H2CO3 |
| ����ƽ�ⳣ�� | 1.75��10-5 | 3.0��10-8 | K1=4.4��10-7 K2=4.7��10-11 |
| A�������ʵ���Ũ�ȵĸ���ҺpH��ϵΪ��pH��NaClO����pH��Na2CO3����pH��NaHCO3����pH��CH3COONa�� |
| B����NaClO��Һ��ͨ������CO2���巴ӦΪ��ClO-+H2O+CO2=HClO+HCO3- |
| C�������ʵ���Ũ�ȵ�HClOϡ��Һ��NaOHϡ��Һ�������Ϻ���Һ�У�c��Na+����c��ClO-����c��OH-����c��H+�� |
| D��Na2CO3��NaHCO3���Һ�У�һ���У�c��Na+��+c��H+��=c��OH-��+c��HCO3-��+c��CO32-�� |
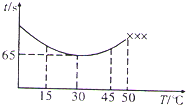 NaHSO4�ɱ�����KIO3��������NaHSO3����ȫ����ʱ����I2������ij�������õ�����ָʾ����ͨ���ⶨ��Һ��������ʱ����̽��Ӱ�컯ѧ��Ӧ���ʵ����أ�
NaHSO4�ɱ�����KIO3��������NaHSO3����ȫ����ʱ����I2������ij�������õ�����ָʾ����ͨ���ⶨ��Һ��������ʱ����̽��Ӱ�컯ѧ��Ӧ���ʵ����أ�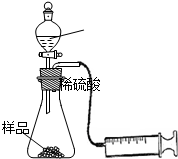 ijѧУ��ѧ����С������������ϻ��������Ϣ��NaHCO3�ڳ�ʪ�Ŀ����лỺ���ֽ��Na2CO3��H2O��CO2��Ϊ����֤��һ��Ϣ���ÿ���С�齫һƿ�ڳ�ʪ�����о��õ�NaHCO3��Ʒ��Ͼ��Ⱥ�������ʵ�飺
ijѧУ��ѧ����С������������ϻ��������Ϣ��NaHCO3�ڳ�ʪ�Ŀ����лỺ���ֽ��Na2CO3��H2O��CO2��Ϊ����֤��һ��Ϣ���ÿ���С�齫һƿ�ڳ�ʪ�����о��õ�NaHCO3��Ʒ��Ͼ��Ⱥ�������ʵ�飺