题目内容
在“部分酸碱盐溶解性表”中存在“碳酸亚铁”。某学习小组设计实验探究碳酸亚铁的性质。
(一)制备碳酸亚铁。
将一定量新制备的硫酸亚铁溶液和过量的碳酸氢铵溶液混合产生大量沉淀和气体。
(1)写出离子方程式: 。
(二)探究碳酸亚铁的热稳定性(加热仪器省略)
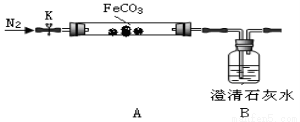
连接仪器、装药品。打开K,先通入一段时间氮气,然后,用酒精喷灯在A处加热玻璃管,观察B瓶溶液变浑浊。待固体分解完后,继续通入氮气至玻璃管冷却。
(2)先通入氮气的目的是 。B瓶现象能说明 。
(3)停止加热之前,是否拆开A、B之间橡胶管?答: ;理由是 。
(三)探究碳酸亚铁还原性
【查阅资料】①氧化亚铁是一种黑色粉末,它不稳定,在空气中加热,就迅速被氧化成四氧化三铁。②碳酸亚铁在空气中灼烧生成氧化铁。
(4)探究碳酸亚铁和氧气反应的固体成分:
①【提出设想】假设1 固体成分是氧化铁;
假设2 固体成分是四氧化三铁;
假设3 。
②【实验验证】连接仪器、装药品,打开止水夹K,通入氧气,加热玻璃管。Y瓶中澄清石灰水不产生沉淀时,停止加热,继续通入氧气至玻璃管冷却。
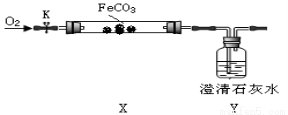
取少量玻璃管里固体于试管,滴加稀硫酸,微热,固体完全溶解。将溶液分成甲、乙两份溶液,进行后续实验。
实验编号 | 实验步骤 | 实验现象 |
i | 向甲溶液滴加KSCN溶液 | 溶液变红色 |
ii | 向乙溶液滴加酸性高锰酸钾溶液 | 溶液不褪色 |
【实验评价】上述实验 (填:i或ii)不能确定样品成分。
【实验结论】根据上述实验结果,该小组得到碳酸亚铁在氧气中高温灼烧得到产物是 。
(5)定量探究:取23.2g纯净固体碳酸亚铁,在空气中高温灼烧至恒重,称得固体质量净减7.2g。通过计算确定固体成分是 。
(9分)
(1)Fe2+ +2HCO3- =FeCO3↓+H2O+CO2↑ (1分)
(2)排尽装置内空气,避免氧气干扰(1分) 分解产物有二氧化碳(1分)
(3)否(1分) 通入氮气,玻璃管内气压不会减少(1分)
(4)固体成分是氧化铁和四氧化三铁(1分) i(1分) 氧化铁和二氧化碳(1分)
(5)氧化铁(1分)
【解析】
试题分析:(1)新制备的硫酸亚铁溶液和过量的碳酸氢铵溶液混合产生大量沉淀和气体,该沉淀是碳酸亚铁沉淀,气体应是二氧化碳,离子方程式为Fe2+ +2HCO3- =FeCO3↓+H2O+CO2↑;
(2)因为亚铁盐极易被氧化,所以通入氮气的目的是排除空气中的氧气,以免造成干扰;B瓶变浑浊,说明碳酸亚铁的分解产物中有二氧化碳气体;
(3)否,因为分解完全后悔继续通入氮气直到玻璃管冷却,所以该过程中玻璃管内气压不会减少,不会发生倒吸现象;
(4)根据查阅的资料判断假设3应是氧化铁和四氧化三铁的混合物;上述实验i不能确定固体的成分,因为无论是哪种假设,溶于酸后溶液中都存在铁离子,加入KSCN溶液后都会变红色,实验不能判断固体的成分,而实验ii中的现象是酸性高锰酸钾溶液不褪色,说明该溶液中不含有亚铁离子,所以该固体的成分是氧化铁;Y瓶产生沉淀,说明产物中还有二氧化碳,所以该小组得到碳酸亚铁在氧气中高温灼烧得到产物是氧化铁和二氧化碳;
(5)23.2g纯净固体碳酸亚铁的物质的量是0.2mol,则加热后的固体中铁元素的物质的量是0.2mol,由题意可知剩余固体的质量是23.2-7.2=16g,其中铁元素的质量是11.2g,则O元素的质量是16-11.2=4.8g,O元素的物质的量是0.3mol,所以剩余固体中Fe与O元素的物质的量之比是2:3,所以该固体是氧化铁。
考点:考查对反应流程的分析,对实验的评价,离子方程式的书写,物质成分的确定

 ”的且只含一个官能团的同分异构体有( )。
”的且只含一个官能团的同分异构体有( )。