题目内容
2.设NA表示阿伏伽德罗常数的值,下列说法正确的是( )| A. | 80℃时,1L pH=1的硫酸溶液中,含有的OH-数目为10-13NA | |
| B. | 含0.1mol NH4HSO4的溶液中,阳离子数目略小于0.2NA | |
| C. | C3H8分子中的2个H原子分别被1个-NH3和1个-OH取代,1mol此有机物所含共同电子对数目为13NA | |
| D. | 以Mg、Al为电极,NaOH溶液为电解质溶液的原电池中,导线上流过NA个电子 |
分析 A、80℃时水的离子积Kw大于10-14;
B、在含0.1mol NH4HSO4的溶液中,存在电荷守恒:n(NH4+)+n(H+)=n(OH-)+2n(SO42-);
C、C3H8分子中的2个H原子分别被1个-NH2和1个-OH取代后,比丙烷多了3条共价键;
D、以Mg、Al为电极,NaOH溶液为电解质溶液的原电池,负极铝的质量不明确.
解答 解:A、80℃时水的离子积Kw大于10-14,故pH=1的硫酸溶液中,氢氧根的浓度大于10-13mol/L,故溶液中氢氧根的个数大于10-13NA个,故A错误;
B、在含0.1mol NH4HSO4的溶液中,硫酸根的物质的量为0.1mol,而此溶液中存在电荷守恒:n(NH4+)+n(H+)=n(OH-)+2n(SO42-),故溶液中的阳离子的物质的量大于0.2mol,故B错误;
C、C3H8分子中的2个H原子分别被1个-NH2和1个-OH取代后,比丙烷多了3条共价键,而丙烷中含10条共价键,故取代后所得的产物中含13条共价键,即1mol此物质含13NA对共用电子对,故C正确;
D、以Mg、Al为电极,NaOH溶液为电解质溶液的原电池,负极铝的质量不明确,故反应掉的铝的质量不明确,则转移的电子个数无法计算,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意公式的运用和物质的结构特点.

练习册系列答案
相关题目
12.某有机物Q的结构简式如图,下列有关Q的说法正确的是( )
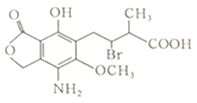

| A. | 分子式为C14H25O6NBr | |
| B. | 该分子中含有两个手性碳原子 | |
| C. | 不能使酸性高锰酸钾溶液褪色 | |
| D. | Q在一定条件下与氢氧化钠溶液反应,1molQ最多消耗3molNaOH |
13.有四种短周期的主族元素X、Y、Z、W.X的一种原子常用于鉴定文物的年代,Y是地壳中含量最多的金属元素,W的原子核外某两层电子数目之比为4:3,X和Z同族.下列说法中正确的是( )
| A. | 简单离子半径:Y>W | |
| B. | 上述四种元素的单质中只有2种能导电 | |
| C. | X与Z两者的最高价氧化物的组成和结构相似 | |
| D. | 在加热条件下,Y的单质可溶于W的最高价含氧酸的浓溶液中 |
10.化学与生活、生产、可持续发展密切相关,下列说法正确的是( )
| A. | 14C可用于文物年代的鉴定,14C和12C互为同素异形体 | |
| B. | 在日常生活中,化学腐蚀是造成钢铁腐蚀的主要原因 | |
| C. | 现代工业生产中芳香烃主要来源于石油化工的催化重整和煤的干馏 | |
| D. | 高纯度的SiO2可以制成光电池将光能直接转换为化学能 |
14.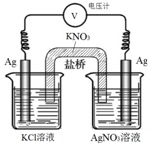 一定条件下,实验室利用如图所示装置,通过测量电压求算Ksp(AgCl).工作一段时间后,两电极质量均增大.下列说法正确的是( )
一定条件下,实验室利用如图所示装置,通过测量电压求算Ksp(AgCl).工作一段时间后,两电极质量均增大.下列说法正确的是( )
 一定条件下,实验室利用如图所示装置,通过测量电压求算Ksp(AgCl).工作一段时间后,两电极质量均增大.下列说法正确的是( )
一定条件下,实验室利用如图所示装置,通过测量电压求算Ksp(AgCl).工作一段时间后,两电极质量均增大.下列说法正确的是( )| A. | 右池中的银电极作负极 | B. | 总反应为Ag++Cl-=AgCl | ||
| C. | 正极反应为Ag-e-=Ag+ | D. | 盐桥中的NO3-向右池方向移动 |
11.水是自然界最重要的分散剂,关于水的叙述错误的是( )
| A. | 水分子是含极性键的极性分子 | |
| B. | 水的电离方程式为:H2O?2H++O2- | |
| C. | 重水(D2O)分子中,各原子质量数之和是质子数之和的两倍 | |
| D. | 相同质量的水具有的内能:固体<液体<气体 |
11.25℃时,下列各组离子在指定溶液中可能大量共存的是( )
| A. | pH=1的溶液中:Na+、K+、MnO4-、CO32- | |
| B. | 无色溶液中:Cu2+、Al3+、NH4+、Cl- | |
| C. | 由水电离出的c(H+)=1×10-13mol•L-1的溶液中:Mg2+、Cu2+、SO42-、NO3- | |
| D. | 0.1mol•L-1FeCl3溶液中:Fe2+、NH4+、SCN-、SO42- |
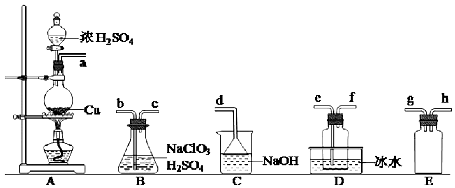
 .
.


