题目内容
下表为元素周期表的一部分:
I.请参照元素①-⑥在表中的位置,用化学用语回答下列问题:
(1)写出元素②的离子结构示意图 .
(2)②、③、⑤的离子半径由大到小的顺序为 .
(3)元素④与⑥形成化合物的电子式是 .
Ⅱ.由上述部分元素组成的物质间,在一定条件下,可以发生下图所示的变化,其中A是一种淡黄色固体.请回答:

(4)写出固体A与液体X反应的离子方程式 .
(5)气体Y是一种大气污染物,直接排放会形成酸雨.可用溶液B吸收,当B与Y物质的量之比为1:1且恰好完全反应时,所得溶液D.已知溶液D显酸性,则D溶液中各种离子浓度由大到小的顺序为
(6)在500℃,101kPa时,气体C与气体Y反应生成0.2mol气体E时,放出akJ热量,写出该条件下反应的热化学方程式 .
(7)若气体C与Y在恒容绝热的条件下反应,下列说法能判断达到平衡状态的是 .
A.温度不变 B.气体总压强不变 C.混合气体的密度不变 D.混合气体的平均分子量不变.
| 族 周期 | ||||||||
| 1 | ① | |||||||
| 2 | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ||||
(1)写出元素②的离子结构示意图
(2)②、③、⑤的离子半径由大到小的顺序为
(3)元素④与⑥形成化合物的电子式是
Ⅱ.由上述部分元素组成的物质间,在一定条件下,可以发生下图所示的变化,其中A是一种淡黄色固体.请回答:

(4)写出固体A与液体X反应的离子方程式
(5)气体Y是一种大气污染物,直接排放会形成酸雨.可用溶液B吸收,当B与Y物质的量之比为1:1且恰好完全反应时,所得溶液D.已知溶液D显酸性,则D溶液中各种离子浓度由大到小的顺序为
(6)在500℃,101kPa时,气体C与气体Y反应生成0.2mol气体E时,放出akJ热量,写出该条件下反应的热化学方程式
(7)若气体C与Y在恒容绝热的条件下反应,下列说法能判断达到平衡状态的是
A.温度不变 B.气体总压强不变 C.混合气体的密度不变 D.混合气体的平均分子量不变.
考点:无机物的推断,元素周期律和元素周期表的综合应用
专题:推断题,元素周期律与元素周期表专题
分析:I.根据元素在周期表中的位置知,①②③④⑤⑥分别是H、O、Na、Si、S、Cl元素,
(1)元素②的离子核外有2个电子层、最外层有8个电子,核内有8个质子;
(2)离子的电子层数越多,其离子半径越大,电子层结构相同的离子,其离子半径随着原子序数增大而减小;
(3)元素④与⑥形成化合物为SiCl4,属于共价化合物,硅原子和每个Cl原子之间都存在共价键;
II.由上述部分元素组成的物质,A是一种淡黄色固体,则A为Na2O2,能与液态X反应生成气体C与B的溶液,可推知X为H2O、B为NaOH、C为O2,
(4)过氧化钠和水反应生成NaOH和氧气;
(5)气体Y是一种大气污染物,直接排放会形成酸雨,则Y是二氧化硫,当B与Y物质的量之比为1:1且恰好完全反应时,所得溶液D,则D为NaHSO3,溶液D显酸性,说明亚硫酸氢根离子电离程度大于水解程度,再结合电荷守恒判断离子浓度大小;
(6)在500℃,101kPa时,二氧化硫和氧气反应生成三氧化硫,所以E是三氧化硫、F是硫酸,气体C与气体Y反应生成0.2mol气体E时,放出akJ热量,则2mol二氧化硫完全反应放出10akJ热量,据此书写热化学反应方程式;
(7)当反应前后改变的物理量不变时,该反应达到平衡状态,据此判断.
(1)元素②的离子核外有2个电子层、最外层有8个电子,核内有8个质子;
(2)离子的电子层数越多,其离子半径越大,电子层结构相同的离子,其离子半径随着原子序数增大而减小;
(3)元素④与⑥形成化合物为SiCl4,属于共价化合物,硅原子和每个Cl原子之间都存在共价键;
II.由上述部分元素组成的物质,A是一种淡黄色固体,则A为Na2O2,能与液态X反应生成气体C与B的溶液,可推知X为H2O、B为NaOH、C为O2,
(4)过氧化钠和水反应生成NaOH和氧气;
(5)气体Y是一种大气污染物,直接排放会形成酸雨,则Y是二氧化硫,当B与Y物质的量之比为1:1且恰好完全反应时,所得溶液D,则D为NaHSO3,溶液D显酸性,说明亚硫酸氢根离子电离程度大于水解程度,再结合电荷守恒判断离子浓度大小;
(6)在500℃,101kPa时,二氧化硫和氧气反应生成三氧化硫,所以E是三氧化硫、F是硫酸,气体C与气体Y反应生成0.2mol气体E时,放出akJ热量,则2mol二氧化硫完全反应放出10akJ热量,据此书写热化学反应方程式;
(7)当反应前后改变的物理量不变时,该反应达到平衡状态,据此判断.
解答:
解:I.根据元素在周期表中的位置知,①②③④⑤⑥分别是H、O、Na、Si、S、Cl元素,
(1)元素②的离子核外有2个电子层、最外层有8个电子,核内有8个质子,其离子结构示意图为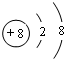 ,故答案为:
,故答案为: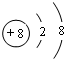 ;
;
(2)离子的电子层数越多,其离子半径越大,电子层结构相同的离子,其离子半径随着原子序数增大而减小,所以离子半径大小顺序是S2->O2->Na+,
故答案为:S2->O2->Na+;
(3)元素④与⑥形成化合物为SiCl4,属于共价化合物,硅原子和每个Cl原子之间都存在共价键,其电子式为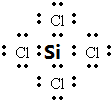 ,
,
故答案为: ;
;
II.由上述部分元素组成的物质,A是一种淡黄色固体,则A为Na2O2,能与液态X反应生成气体C与B的溶液,可推知X为H2O、B为NaOH、C为O2,
(4)过氧化钠和水反应生成NaOH和氧气,离子方程式为2Na2O2+2H2O=4Na++4OH-+O2↑,故答案为2Na2O2+2H2O=4Na++4OH-+O2↑;
(5)气体Y是一种大气污染物,直接排放会形成酸雨,则Y是二氧化硫,当B与Y物质的量之比为1:1且恰好完全反应时,所得溶液D,则D为NaHSO3,溶液D显酸性,说明亚硫酸氢根离子电离程度大于水解程度,钠离子不水解,水和亚硫酸氢根离子电离生成氢离子,所以离子浓度大小顺序是c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>(OH-),故答案为:c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>(OH-);
(6)在500℃,101kPa时,二氧化硫和氧气反应生成三氧化硫,所以E是三氧化硫、F是硫酸,气体C与气体Y反应生成0.2mol气体E时,放出akJ热量,则2mol二氧化硫完全反应放出10akJ热量,其热化学反应方程式为2SO2+O2?2SO3△H=-10akJ/mol,故答案为:2SO2+O2?2SO3△H=-10akJ/mol;
(7)当反应前后改变的物理量不变时,该反应达到平衡状态,该可逆反应前后改变的物理量有温度、压强、平均分子量,所以当温度、压强、混合气体的平均分子量不变时,该反应达到平衡状态,故选ABD.
(1)元素②的离子核外有2个电子层、最外层有8个电子,核内有8个质子,其离子结构示意图为
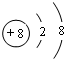 ,故答案为:
,故答案为: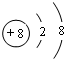 ;
;(2)离子的电子层数越多,其离子半径越大,电子层结构相同的离子,其离子半径随着原子序数增大而减小,所以离子半径大小顺序是S2->O2->Na+,
故答案为:S2->O2->Na+;
(3)元素④与⑥形成化合物为SiCl4,属于共价化合物,硅原子和每个Cl原子之间都存在共价键,其电子式为
 ,
,故答案为:
 ;
;II.由上述部分元素组成的物质,A是一种淡黄色固体,则A为Na2O2,能与液态X反应生成气体C与B的溶液,可推知X为H2O、B为NaOH、C为O2,
(4)过氧化钠和水反应生成NaOH和氧气,离子方程式为2Na2O2+2H2O=4Na++4OH-+O2↑,故答案为2Na2O2+2H2O=4Na++4OH-+O2↑;
(5)气体Y是一种大气污染物,直接排放会形成酸雨,则Y是二氧化硫,当B与Y物质的量之比为1:1且恰好完全反应时,所得溶液D,则D为NaHSO3,溶液D显酸性,说明亚硫酸氢根离子电离程度大于水解程度,钠离子不水解,水和亚硫酸氢根离子电离生成氢离子,所以离子浓度大小顺序是c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>(OH-),故答案为:c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>(OH-);
(6)在500℃,101kPa时,二氧化硫和氧气反应生成三氧化硫,所以E是三氧化硫、F是硫酸,气体C与气体Y反应生成0.2mol气体E时,放出akJ热量,则2mol二氧化硫完全反应放出10akJ热量,其热化学反应方程式为2SO2+O2?2SO3△H=-10akJ/mol,故答案为:2SO2+O2?2SO3△H=-10akJ/mol;
(7)当反应前后改变的物理量不变时,该反应达到平衡状态,该可逆反应前后改变的物理量有温度、压强、平均分子量,所以当温度、压强、混合气体的平均分子量不变时,该反应达到平衡状态,故选ABD.
点评:本题考查了无机物推断及元素周期表、元素周期律的综合应用,综合性较强,涉及元素化合物知识、化学反应原理、化学用语等知识点,难点是化学平衡状态判断,注意题干中限制性信息,为易错点.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
下列不属于合成纤维的是( )
| A、的确良 | B、棉花 |
| C、人造棉花 | D、氯纶 |
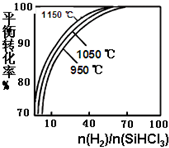 粗硅提纯常见方法之一是先将粗硅与HCl制得SiHCl3,经提纯后再用H2还原:SiHCl3(g)+H2(g)?Si(s)+3HCl(g)不同温度及不同n(H2)/n(SiHCl3)时,反应物X的平衡转化率关系如图;
粗硅提纯常见方法之一是先将粗硅与HCl制得SiHCl3,经提纯后再用H2还原:SiHCl3(g)+H2(g)?Si(s)+3HCl(g)不同温度及不同n(H2)/n(SiHCl3)时,反应物X的平衡转化率关系如图; 美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电源,其构造如图所示:a、b两个极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电.
美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电源,其构造如图所示:a、b两个极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电.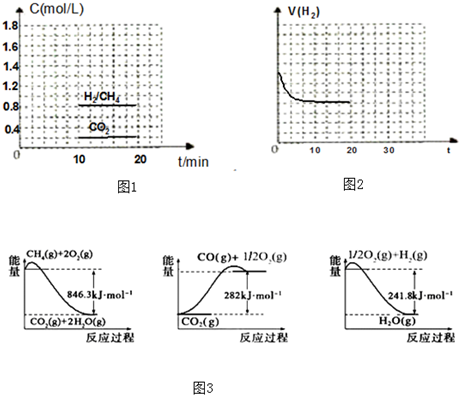
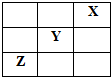 X、Y、Z是Ⅳ~ⅦA族的三种非金属元素,它们在周期表中的位置如图所示.试回答:
X、Y、Z是Ⅳ~ⅦA族的三种非金属元素,它们在周期表中的位置如图所示.试回答: