题目内容
根据反应2KMnO4+10FeSO4+8H2SO4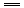 2MnSO4+5Fe2(SO4)3+K2SO4+8H2O,可用作与酸碱中和滴定相同的仪器和操作方法测定绿矾中FeSO4的质量分数.
2MnSO4+5Fe2(SO4)3+K2SO4+8H2O,可用作与酸碱中和滴定相同的仪器和操作方法测定绿矾中FeSO4的质量分数.
实验步骤顺序如下:
①称取绿矾样品W g,配成100mL溶液.
②取25.0mL待测液,置于锥形瓶中,再加入适量H2SO4溶液供滴定使用.
③将m mol/L的标准KMnO4溶液装入滴定液,调节液面刻度至a mL处.
④用标准KMnO4溶液滴定待测液.
⑤该实验是用反应物自身颜色变化指示反应终点,到滴定终点时,滴定管内液面的高度为b mL.
⑥重复滴定操作2~3次.
⑦计算.
请根据以上实验步骤填写有关内容.
(1)实验步骤①中,应从下列仪器中选取的仪器是________.
A.托盘天平(含砝码、镊子)
B.50mL酸式滴定管
C.100mL量筒
D.100mL容量瓶
E.烧杯
F.胶头滴管
G.锥形瓶
H.玻璃棒
L.V形纸槽
J.药匙
(2)不能用________式滴定管盛放KMnO4溶液,其原因是________.
(3)锥形瓶用蒸馏水洗净的标志是________;若锥形瓶未干燥,对实验结果的影响是:________(填“偏高”、“偏低”、“无影响”).
(4)滴定时,两眼应注视________.
(5)绿矾中FeSO4的质量分数为(FeSO4%)________.
解析:
|
(1)A D E F H J;(2)碱,KMnO4有强氧化性,会腐蚀碱式滴定管下端的橡皮管;(3)瓶壁上无水珠挂着,无影响;(4)锥形瓶中溶液颜色的变化;(5) 导解:(1)配制一定物质的量浓度的FeSO4溶液. (5)消耗的KMnO4的物质的量为: (b-a)×10-3×m mol,由反应方程式知FeSO4总的物质的量为:5×(b-a)×10-3×m×4=2m(b-a)×10-2mol 故FeSO4%= |


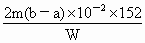 ×100%.
×100%.


