��Ŀ����
��������Դ��ʹ�����ȼ�ϣ����Դﵽ�����Ч��������Ⱦ��Ŀ�ģ�
��1����C��H��O����Ԫ���е����ֺ����ֱַ���ɵ�ȼ�����ʼ��ң�������о���������1���ҷ����к���18�����ӣ�����ҷֱ��� ��
����һ�����ȼ�ϣ���ҵ�Ͽ��ü�������Ӧ�Ƶã�
��T1�¶�ʱ�������Ϊ2L���ܱ������г���2mol��6mol H2����Ӧ�ﵽƽ����c���ף�=0.2mol/L��������ƽ��ʱ�����ʵ����� mol��
�������¶ȵ�T2ʱ����Ӧ�Ĵﵽƽ������д�ʩ�������ת���ʵ��� ��������ĸ��
A������2mol�� B�����뵪�� C��������� D���������������һ��
��2������Ҳ��һ�����ȼ�ϣ�������ȫȼ��ʱ��Ч�ʽ��Ͳ�������ж����������Ⱦ����֪��
CH4��g��+2O2��g��=CO2��g��+2H2O��l����H1=-890.3kJ/mol
2CO ��g��+O2��g��=2CO2��g����H2=-566.0kJ/mol
����鲻��ȫȼ������һ����̼��Һ̬ˮʱ���Ȼ�ѧ����ʽΪ�� ��
��3������ȼ�ϵ�ؿ����������������ʣ���ͼ�����ü���ȼ�ϵ�ص��50mL 2mol/L���Ȼ�ͭ��Һ��װ��ʾ��ͼ��
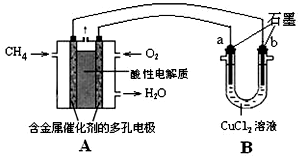
��ش��������⣺
�ټ���ȼ�ϵ�صĸ�����Ӧʽ�ǣ� ��
�ڵ���·����0.1mol����ͨ��ʱ�� ���a����b���������� g��
��4��̼���ȹ㷺Ӧ���ڵ��ӹ�ҵ��������ʯ����Ҫ�ɷ�ΪSrSO4��Ϊ����ԭ���Ʊ�̼���ȣ�����֪��
Ksp��SrSO4��=3.2��10-7��Ksp��SrCO3��=1.1��10-10����
�ٽ�����ʯ�����Na2CO3��Һ������ȡ����ȣ����������ӷ�Ӧ����ʽΪ��SrSO4+CO32-=SrCO3+SO42-
�ڵ�ת�����ʱ�����Һ��c��CO32-��=1.0��10-3mol/L��c��SO42-��= mol/L��
��1����C��H��O����Ԫ���е����ֺ����ֱַ���ɵ�ȼ�����ʼ��ң�������о���������1���ҷ����к���18�����ӣ�����ҷֱ���
����һ�����ȼ�ϣ���ҵ�Ͽ��ü�������Ӧ�Ƶã�
��T1�¶�ʱ�������Ϊ2L���ܱ������г���2mol��6mol H2����Ӧ�ﵽƽ����c���ף�=0.2mol/L��������ƽ��ʱ�����ʵ�����
�������¶ȵ�T2ʱ����Ӧ�Ĵﵽƽ������д�ʩ�������ת���ʵ���
A������2mol�� B�����뵪�� C��������� D���������������һ��
��2������Ҳ��һ�����ȼ�ϣ�������ȫȼ��ʱ��Ч�ʽ��Ͳ�������ж����������Ⱦ����֪��
CH4��g��+2O2��g��=CO2��g��+2H2O��l����H1=-890.3kJ/mol
2CO ��g��+O2��g��=2CO2��g����H2=-566.0kJ/mol
����鲻��ȫȼ������һ����̼��Һ̬ˮʱ���Ȼ�ѧ����ʽΪ��
��3������ȼ�ϵ�ؿ����������������ʣ���ͼ�����ü���ȼ�ϵ�ص��50mL 2mol/L���Ȼ�ͭ��Һ��װ��ʾ��ͼ��

��ش��������⣺
�ټ���ȼ�ϵ�صĸ�����Ӧʽ�ǣ�
�ڵ���·����0.1mol����ͨ��ʱ��
��4��̼���ȹ㷺Ӧ���ڵ��ӹ�ҵ��������ʯ����Ҫ�ɷ�ΪSrSO4��Ϊ����ԭ���Ʊ�̼���ȣ�����֪��
Ksp��SrSO4��=3.2��10-7��Ksp��SrCO3��=1.1��10-10����
�ٽ�����ʯ�����Na2CO3��Һ������ȡ����ȣ����������ӷ�Ӧ����ʽΪ��SrSO4+CO32-=SrCO3+SO42-
�ڵ�ת�����ʱ�����Һ��c��CO32-��=1.0��10-3mol/L��c��SO42-��=
���㣺��ѧƽ��ļ���,�ø�˹���ɽ����йط�Ӧ�ȵļ���,ԭ��غ͵��صĹ���ԭ��,��ѧƽ���Ӱ������,���ܵ���ʵ��ܽ�ƽ�⼰����ת���ı���
ר�⣺
��������1����C��H��O����Ԫ���е����ֺ����ֱַ���ɵ�ȼ�����ʼ��ң�1���ҷ����к���18�����ӣ����ҷ����к���1��Cԭ�ӡ�1��Oԭ�ӣ�����Hԭ����ĿΪ18-6-8=4������ΪCH3OH�������о��������ʼ�ΪCO��
�١�������ӦCO ��g��+2H2��g��?CH3OH��g����Ӧ�ﵽƽ����c���ף�=0.2mol/L����ƽ��ʱn���ף�=2L��0.2mol/L=0.4mol���ݴ˸�������ʽ����ƽ��ʱ��������ʵ������ݴ˽��
�ڡ����ת���ʣ�Ӧ�ı�����ʹƽ��������Ӧ�ƶ�������T1�¶�ʱƽ�ⳣ������T2�¶ȵ�ƽ�ⳣ������жϸ÷�Ӧ�ķ�Ӧ�ȣ��ж��¶ȶԷ�Ӧ��Ӱ�죬ע�ⲻ��ֻ�����Ũ�ȣ�
��2�����ݸ�˹������д���鲻��ȫȼ������һ����̼��Һ̬ˮʱ���Ȼ�ѧ����ʽ��
��3���١�ԭ��ظ�������������Ӧ�������ڸ���ͨ�룬���������£�����������Ӧ����CO2��H+��
�ڡ�BΪ���أ�ͭ���ӷ�����ԭ��Ӧ���������������ü�����ԭ��صĸ���������ת�Ƶ��Ӽ�������Cu�����ʵ������ٸ���m=nM��������Cu��������
��4���ڵ�ת�����ʱ������Ksp��SrCO3������c��Sr2+�����ٸ���Ksp��SrSO4������c��SO42-����
�١�������ӦCO ��g��+2H2��g��?CH3OH��g����Ӧ�ﵽƽ����c���ף�=0.2mol/L����ƽ��ʱn���ף�=2L��0.2mol/L=0.4mol���ݴ˸�������ʽ����ƽ��ʱ��������ʵ������ݴ˽��
�ڡ����ת���ʣ�Ӧ�ı�����ʹƽ��������Ӧ�ƶ�������T1�¶�ʱƽ�ⳣ������T2�¶ȵ�ƽ�ⳣ������жϸ÷�Ӧ�ķ�Ӧ�ȣ��ж��¶ȶԷ�Ӧ��Ӱ�죬ע�ⲻ��ֻ�����Ũ�ȣ�
��2�����ݸ�˹������д���鲻��ȫȼ������һ����̼��Һ̬ˮʱ���Ȼ�ѧ����ʽ��
��3���١�ԭ��ظ�������������Ӧ�������ڸ���ͨ�룬���������£�����������Ӧ����CO2��H+��
�ڡ�BΪ���أ�ͭ���ӷ�����ԭ��Ӧ���������������ü�����ԭ��صĸ���������ת�Ƶ��Ӽ�������Cu�����ʵ������ٸ���m=nM��������Cu��������
��4���ڵ�ת�����ʱ������Ksp��SrCO3������c��Sr2+�����ٸ���Ksp��SrSO4������c��SO42-����
���
�⣺��1����C��H��O����Ԫ���е����ֺ����ֱַ���ɵ�ȼ�����ʼ��ң�1���ҷ����к���18�����ӣ����ҷ����к���1��Cԭ�ӡ�1��Oԭ�ӣ�����Hԭ����ĿΪ18-6-8=4������ΪCH3OH�������о��������ʼ�ΪCO��
�ʴ�Ϊ��CO��CH3OH��
�١�������ӦCO ��g��+2H2��g��?CH3OH��g����Ӧ�ﵽƽ����c���ף�=0.2mol/L����ƽ��ʱn���ף�=2L��0.2mol/L=0.4mol����
CO ��g��+2H2��g��?CH3OH��g����
��ʼ��mol����2 6 0
�仯��mol����1.6 3.2 1.6
ƽ�⣨mol����0.4 2.8 1.6
����ƽ��ʱ�����ʵ�����1.6mol���ʴ�Ϊ��1.6��
�ڡ��÷�ӦΪ���ȷ�Ӧ��
A������2mol�ף�ƽ��������Ӧ�ƶ�������ת���ʽ��ͣ���A����
B�����뵪������Ӧ��������ֵ�Ũ�Ȳ��䣬ƽ�ⲻ�ƶ�����ת���ʲ��䣬��B����
C��������ң�ƽ��������Ӧ�ƶ�����ת��������C��ȷ��
D���������������һ�룬����ѹǿ��ƽ��������Ӧ�����ƶ�����ת��������D��ȷ��
�ʴ�Ϊ��CD��
��2����֪���١�CH4��g��+2O2��g��=CO2��g��+2H2O��l����H=-890.3kJ?mol-1��
�ڡ�2CO��g��+O2��g��=2CO2��g����H=-566.0kJ?mol-1��
���ø�˹���ɣ��١�2-�ڿɵã�2CH4��g��+3O2��g��=2CO��g��+4H2O��l������H=-1214.6kJ?mol -1
�ʴ�Ϊ��2CH4��g��+3O2��g��=2CO��g��+4H2O��l������H=-1214.6kJ?mol -1��
��3���١�ԭ��ظ�������������Ӧ�������ڸ���ͨ�룬���������£�����������Ӧ����CO2��H+�������缫��ӦʽΪ��CH4-8e-+2H2O=CO2+8H+��
�ʴ�Ϊ��CH4-8e-+2H2O=CO2+8H+��
�ڡ�BΪ���أ�ͭ���ӷ�����ԭ��Ӧ���������������ü�����ԭ��صĸ���������b�缫����Cu��b�缫���������أ�ת��0.1mol���ӣ�����ͭ�����ʵ���Ϊ
=0.05mol��������ͭ������Ϊ0.05mol��64g/mol=3.2g��
�ʴ�Ϊ��b��3.2��
��4����Ksp��SrSO4��=3.2��10-7��Ksp��SrCO3��=1.1��10-10����ת�����ʱ�����Һ��c��CO32-��=1.0��10-3mol/L��
����c��Sr2+��=
=1.1��10-7mol/L��c��SO42-��=
=2.91mol/L��
�ʴ�Ϊ��2.91��
�ʴ�Ϊ��CO��CH3OH��
�١�������ӦCO ��g��+2H2��g��?CH3OH��g����Ӧ�ﵽƽ����c���ף�=0.2mol/L����ƽ��ʱn���ף�=2L��0.2mol/L=0.4mol����
CO ��g��+2H2��g��?CH3OH��g����
��ʼ��mol����2 6 0
�仯��mol����1.6 3.2 1.6
ƽ�⣨mol����0.4 2.8 1.6
����ƽ��ʱ�����ʵ�����1.6mol���ʴ�Ϊ��1.6��
�ڡ��÷�ӦΪ���ȷ�Ӧ��
A������2mol�ף�ƽ��������Ӧ�ƶ�������ת���ʽ��ͣ���A����
B�����뵪������Ӧ��������ֵ�Ũ�Ȳ��䣬ƽ�ⲻ�ƶ�����ת���ʲ��䣬��B����
C��������ң�ƽ��������Ӧ�ƶ�����ת��������C��ȷ��
D���������������һ�룬����ѹǿ��ƽ��������Ӧ�����ƶ�����ת��������D��ȷ��
�ʴ�Ϊ��CD��
��2����֪���١�CH4��g��+2O2��g��=CO2��g��+2H2O��l����H=-890.3kJ?mol-1��
�ڡ�2CO��g��+O2��g��=2CO2��g����H=-566.0kJ?mol-1��
���ø�˹���ɣ��١�2-�ڿɵã�2CH4��g��+3O2��g��=2CO��g��+4H2O��l������H=-1214.6kJ?mol -1
�ʴ�Ϊ��2CH4��g��+3O2��g��=2CO��g��+4H2O��l������H=-1214.6kJ?mol -1��
��3���١�ԭ��ظ�������������Ӧ�������ڸ���ͨ�룬���������£�����������Ӧ����CO2��H+�������缫��ӦʽΪ��CH4-8e-+2H2O=CO2+8H+��
�ʴ�Ϊ��CH4-8e-+2H2O=CO2+8H+��
�ڡ�BΪ���أ�ͭ���ӷ�����ԭ��Ӧ���������������ü�����ԭ��صĸ���������b�缫����Cu��b�缫���������أ�ת��0.1mol���ӣ�����ͭ�����ʵ���Ϊ
| 0.1mol |
| 2 |
�ʴ�Ϊ��b��3.2��
��4����Ksp��SrSO4��=3.2��10-7��Ksp��SrCO3��=1.1��10-10����ת�����ʱ�����Һ��c��CO32-��=1.0��10-3mol/L��
����c��Sr2+��=
| 1.1��10 -10 |
| 1.0��10 -3 |
| 3.2��10 -7 |
| 1.1��10 -7 |
�ʴ�Ϊ��2.91��
���������⿼���Ϊ�ۺϣ��漰�����ƶϡ���ѧƽ���йؼ��㡢��ѧƽ�ⳣ�����绯ѧ�Լ���˹���ɵ�Ӧ�õȣ���Ŀ�Ѷ��еȣ�ע������˹���ɵ�Ӧ�ã���3���п��������ܷ�Ӧʽ��������Ӧʽ��д������Ӧʽ��

��ϰ��ϵ�д�
 ��������ѧ����ϵ�д�
��������ѧ����ϵ�д� ��Ԫ������ĩ��ϵ�д�
��Ԫ������ĩ��ϵ�д�
�����Ŀ
�����£���Ũ�ȵ���������и������ʵ���Һ���ʱ��pH��7���ǣ�������
| A��NaCl��CuSO4��Ba��NO3��2 |
| B��AlCl3��NaOH��KNO3 |
| C��K2CO3��HNO3��HCl |
| D��Na2S��HCl��KCl |
����˵����ȷ���ǣ�������
| A��ɫ��ͨ�����ڷ���ṹ������������ʺͻ�ѧ�������Ƶ����ʣ�����ɫ����������һ�� |
| B��������ɺ���Ҫϴ�ӳ�������������©����ֱ�Ӽ�ϴ�Ӽ���Ȼ��ˮ��ͷ��ʹϴ�Ӽ�Ѹ��ͨ������ |
| C����ȡ�����е�Ԫ��ʱ��Ϊ��֤I-��ȫ������ΪI2����ü����������������H2O2��������ˮ�� |
| D��������δ��ȥ����Ĥ����Ƭ�ֱ�Ͷ��1mol?L-1CuSO4��Һ��1mol?L-1CuCl2��Һ�У�����Ƭ�̣���Ƭ���涼�۲첻�����Եķ�Ӧ���� |
����ͬ�¶Ⱥ������Ϊ1L�������ܱ������У������¶Ⱥ��ݻ����䣬�����ֲ�ͬ��Ͷ�Ϸ�ʽ���з�Ӧ��ƽ��ʱ�й��������£���֪��ͬ������2SO2��g��+O2��g��?2SO3��g����H=-196kJ/mol��������˵����ȷ���ǣ�������
| ���� | �� | �� | �� |
| ��ʼͶ���� | 2mol SO2��1mol O2 | 2mol SO3 | 2mol SO2��2mol O2 |
| ��Ӧ�ų������յ� ������kJ�� | Q1 | Q2 | Q3 |
| ƽ��ʱSO3�����ʵ��� | n1 | n2 | n3 |
| ƽ��ת���� | |||
| ƽ��ʱѹǿ | p1 | p2 | p3 |
| A��Q1=Q2��Q3 |
| B��n2��n1��n3 |
| C��a1+a2=1 |
| D��p1��p2��p3 |
 �Իش��������⣺
�Իش��������⣺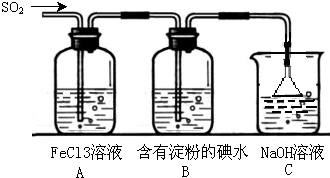 ij��ȤС��̽��SO2���廹ԭFe3+��I2������ʹ�õ�ҩƷ��װ����ͼ��ʾ��
ij��ȤС��̽��SO2���廹ԭFe3+��I2������ʹ�õ�ҩƷ��װ����ͼ��ʾ��