题目内容
写出下列物质电离方程.
(1)H2SO4: ;
(2)H2CO3: ;
(3)HF: .
(1)H2SO4:
(2)H2CO3:
(3)HF:
考点:电离方程式的书写
专题:离子反应专题
分析:先判断强电解质、弱电解质,然后根据强电解质完全电离,电离方程式用等号,弱电解质部分电离,其电离方程式用可逆号进行解答.
解答:
解:(1)硫酸为强电解质,溶液中电离出硫酸根离子和氢离子,其电离方程式为:H2SO4=2H++SO42-,
故答案为:H2SO4=2H++SO42-;
(2)碳酸为二元弱酸,电离过程分步进行,主要以第一步为主,碳酸的电离方程式为:H2CO3?H++HCO3-,
故答案为:H2CO3?H++HCO3-;
(3)氢氟酸为电解质,溶液中部分电离出氢离子和氟离子,氢氟酸的电离方程式为:HF?H++F-,
故答案为:HF?H++F-.
故答案为:H2SO4=2H++SO42-;
(2)碳酸为二元弱酸,电离过程分步进行,主要以第一步为主,碳酸的电离方程式为:H2CO3?H++HCO3-,
故答案为:H2CO3?H++HCO3-;
(3)氢氟酸为电解质,溶液中部分电离出氢离子和氟离子,氢氟酸的电离方程式为:HF?H++F-,
故答案为:HF?H++F-.
点评:本题考查了电离方程式的书写,题目难度中等,主要掌握电离方程式的书写原则,注意碳酸为二元弱酸,电离过程分步进行,电离方程式只写出第一步即可.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)?2NH3(g)+CO2(g);不能判断该分解反应已经达到平衡的是( )
| A、密闭容器中氨气的浓度不变 |
| B、密闭容器中总压强不变 |
| C、密闭容器中混合气体的密度不变 |
| D、2v(NH3)=v(CO2) |
下列说法中正确的是( )
| A、纯净的电解质在固态时全部属于离子晶体 |
| B、CCl4、CS2及BF3三种分子中所有原子都满足最外层8电子稳定结构 |
| C、用道尔顿的原子结构理论无法解释同位素现象 |
| D、化学键相同,则晶体类型也相同 |
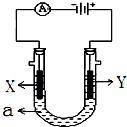 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: