题目内容
17. 在体积为2L的恒容密闭容器中加入0.6mol的CO和H2混合气体,在不同温度下反应CO(g)+2H2O(g)?CH3OH(g)达到平衡,平衡时CH3OH的体积分数随起始n(CO):n(H2)的变化曲线如图所示.则下列结论正确的是( )
在体积为2L的恒容密闭容器中加入0.6mol的CO和H2混合气体,在不同温度下反应CO(g)+2H2O(g)?CH3OH(g)达到平衡,平衡时CH3OH的体积分数随起始n(CO):n(H2)的变化曲线如图所示.则下列结论正确的是( )| A. | 反应CO(g)+2H2O(g)?CH3OH(g)的△H<0 | |
| B. | 图示a点n(CO):n(H2)=0.5,CO转化率最高 | |
| C. | 若在状态Ⅰ和Ⅱ时,再向体系中充入He,重新达到平衡,c(CH3OH,状态Ⅱ)=c(CH3OH,状态Ⅰ) | |
| D. | 正反应速率v正:v正(状态Ⅱ)<v正(状态Ⅲ) |
分析 A.当起始n(CO):n(H2)相同时,升高温度,平衡时CH3OH的体积分数增大,说明平衡正向移动,则正反应为吸热反应;
B.起始n(CO):n(H2)越大,c(CO)的起始浓度越大,在同温同体积条件下,相当于增大压强,平衡正向移动;
C.同温同压下,向体系中充入He,不影响组分浓度,对化学平衡状态无影响;
D.温度升高,化学反应速率增大.
解答 解:A.当起始n(CO):n(H2)相同时,升高温度,平衡时CH3OH的体积分数增大,说明平衡正向移动,则正反应为吸热反应,即反应CO(g)+2H2O(g)?CH3OH(g)的△H>0,故A错误;
B.随着起始n(CO):n(H2)越大,c(CO)的起始浓度越大,在同温同体积条件下,相当于增大压强,平衡正向移动,CO转化率逐渐增大,故B错误;
C.同温同压下,向体系中充入He,不影响组分浓度,对化学平衡状态无影响,因此c(CH3OH,状态Ⅱ)=c(CH3OH,状态Ⅰ),故C正确;
D.状态Ⅱ是200℃,状态Ⅲ是100℃,升高温度,化学反应速率增大,因此v正(状态Ⅱ)>v正(状态Ⅲ),故D错误;
故选C.
点评 本题考查化学平衡状态的建立和平衡移动,为高频考点,B选项为该题的难点,注意同温同压下,增大c(CO)等效于增大压强,题目难度中等.

练习册系列答案
 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目
7.下列化学用语表示正确的是( )
| A. | 乙醇的结构简式:C2H6O | |
| B. | 硫离子的结构示意图: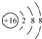 | |
| C. | 氮气的电子式: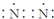 | |
| D. | 氢氧化钡的电离方程式:Ba(OH)2═Ba2++(OH-)2 |
8.设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
| A. | 28g乙烯所含共用电子对数目为4NA | |
| B. | 1mol C4H10分子中共价键总数为13NA | |
| C. | 1 mol甲基所含的电子总数为7NA | |
| D. | 标准状况下,11.2 L己烷所含分子数为0.5 NA |
5.化学与生产、生活密切相关,下列说法正确的是( )
| A. | 明矾是常用的水处理剂,可以用来淡化海水 | |
| B. | 患有胃溃疡的病人的胃酸过多,可以用小苏打医治 | |
| C. | 生活中常用的铝制品与不锈钢制品不易腐蚀,其原理不同 | |
| D. | 食品包装袋中常有硅胶、生石灰、还原铁粉等,其作用完全相同 |
2.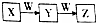 X、Y、Z、W均为中学化学常见物质,且X、Y、Z含有同一种元素,在一定条件下发生如图所示的转化关系,则W不可能是( )
X、Y、Z、W均为中学化学常见物质,且X、Y、Z含有同一种元素,在一定条件下发生如图所示的转化关系,则W不可能是( )
 X、Y、Z、W均为中学化学常见物质,且X、Y、Z含有同一种元素,在一定条件下发生如图所示的转化关系,则W不可能是( )
X、Y、Z、W均为中学化学常见物质,且X、Y、Z含有同一种元素,在一定条件下发生如图所示的转化关系,则W不可能是( )| A. | Al | B. | Si | C. | O2 | D. | Fe |
19.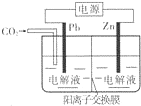 采用电化学法还原CO2是一种使CO2资源化的方法,下图是利用此法制备ZnC2O4的示意图(电解液不参与反应).下列说法正确的是( )
采用电化学法还原CO2是一种使CO2资源化的方法,下图是利用此法制备ZnC2O4的示意图(电解液不参与反应).下列说法正确的是( )
 采用电化学法还原CO2是一种使CO2资源化的方法,下图是利用此法制备ZnC2O4的示意图(电解液不参与反应).下列说法正确的是( )
采用电化学法还原CO2是一种使CO2资源化的方法,下图是利用此法制备ZnC2O4的示意图(电解液不参与反应).下列说法正确的是( )| A. | Zn与电源的负极相连 | |
| B. | ZnC2O4在交换膜右侧生成 | |
| C. | 电解的总反应为:2C02+Zn$\frac{\underline{\;电解\;}}{\;}$ZnC2O4 | |
| D. | 通入11.2 L CO2时,转移0.5 mol电子 |