题目内容
国家卫生部在2000年前就决定逐步使用稳定、高效、无毒的二氧化氯取代氯气消毒饮用水.已知二氧化氯溶于水时有亚氯酸根离子(ClO2-)生成,且氧化产物与还原产物的物质的量之比为1:1.二氧化氯溶于水的反应方程式2ClO2+H2O═HClO3+HClO2,请标明电子转移方向和数目 .
考点:氧化还原反应的电子转移数目计算
专题:
分析:在氧化还原反应中,化合价升高值=化合价降低值=转移电子数,据此回答判断.
解答:
解:反应2ClO2+H2O═HClO3+HClO2中,Cl从+4价升高到了+5价,从+4价降低到了+3价,电子转移为: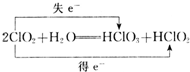 ,故答案为:
,故答案为: .
.
 ,故答案为:
,故答案为: .
.
点评:本题考查学生氧化还原反应中电子转移的方向和数目等知识,属于基本知识的考查,难度不大.

练习册系列答案
相关题目
在含有FeBr2和FeI2的混合溶液中通入足量的氯气,把所得溶液蒸干、灼烧,最后得到的固体是( )
| A、Fe(OH)3 |
| B、FeCl3 |
| C、Fe2O3 |
| D、FeCl3和I2 |
在xR2++yH++O2=mR3++nH2O的离子反应中,化学计量数m的值为( )
| A、2x | ||
| B、4 | ||
C、
| ||
| D、2 |
下列应用或事实与胶体的性质无关的是( )
| A、用明矾净化饮用水 |
| B、用石膏或盐卤制豆腐 |
| C、向FeCl3溶液中滴加NaOH溶液出现红褐色沉淀 |
| D、阳光透过墙上的小孔在较暗的房间里形成一道道光柱 |
现有含金属元素An+的溶液,c(An+)=0.80mol?L-1.取该溶液10mL恰好把20mL 0.40mol?L-1的Na2CO3(aq)中的CO32-全部沉淀.已知上述10mL溶液中含此金属阳离子0.32g,则该金属的相对原子质量为( )
| A、24 | B、32 | C、40 | D、64 |
设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A、0.5molO3与11.2LO2所含的分子数一定相等 |
| B、常温常压下,18g H2O含有的原子总数为3NA |
| C、标准状况下,11.2LCH3CH2OH中含有分子的数目为0.5NA |
| D、1 mol Na 与足量O2 反应,生成Na2O和Na2O2混合物,钠失去NA个电子 |
下列叙述正确的是( )
| A、1 mol H2O的质量为18 g?mol-1 |
| B、3.01×1023个SO2分子的质量为32 g |
| C、CH4的摩尔质量为16 g |
| D、1 mol任何物质均含有6.02×1023个分子 |
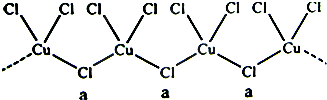
氯和钾与不同价态的铜可生成两种化合物,这两种化合物都可用于催化乙炔聚合,其阴离子均为无限长链结构(如图),a位置上Cl原子的杂化轨道类型为( )

| A、sp杂化 |
| B、sp2杂化 |
| C、sp3杂化 |
| D、dsp2杂化 |
 (1)稀释0.1mol?L-1氨水时,随着水量的增加而减小的是
(1)稀释0.1mol?L-1氨水时,随着水量的增加而减小的是