题目内容
下列实验能达到实验目的是( )
| A、在容量瓶中加入一定体积的水,再加入浓硫酸配制准确浓度的稀硫酸 |
| B、可用四氯化碳萃取出碘水中的碘,但不能用酒精 |
| C、用玻璃棒搅拌漏斗中的液体以加快过滤速度 |
| D、加入盐酸以除去硫酸钠中的少量碳酸钠杂质 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.容量瓶不能做为稀释仪器;
B.根据萃取剂的选择必须符合下列条件:溶质在萃取剂中的溶解度比在原溶剂中要大;萃取剂与原溶剂不相溶;萃取剂与溶质不反应;
C.过滤时,不能用玻璃棒搅拌漏斗中的液体,防止损坏滤纸;
D.加入盐酸引入了新的杂质氯离子.
B.根据萃取剂的选择必须符合下列条件:溶质在萃取剂中的溶解度比在原溶剂中要大;萃取剂与原溶剂不相溶;萃取剂与溶质不反应;
C.过滤时,不能用玻璃棒搅拌漏斗中的液体,防止损坏滤纸;
D.加入盐酸引入了新的杂质氯离子.
解答:
解:A.容量瓶不能做为稀释仪器,是定容仪器,故A错误;
B.碘易溶于四氯化碳,而四氯化碳与水互不相溶,故可以用四氯化碳做萃取剂;乙醇与水互溶,不能做萃取剂,故B正确;
C.过滤时,不能用玻璃棒搅拌漏斗中的液体,故C错误;
D.加入盐酸引入了新的杂质氯离子,不符合除杂原则,故D错误.
故选B.
B.碘易溶于四氯化碳,而四氯化碳与水互不相溶,故可以用四氯化碳做萃取剂;乙醇与水互溶,不能做萃取剂,故B正确;
C.过滤时,不能用玻璃棒搅拌漏斗中的液体,故C错误;
D.加入盐酸引入了新的杂质氯离子,不符合除杂原则,故D错误.
故选B.
点评:本题考查化学实验方案的评价,涉及物质的分离提纯和溶液的稀释等知识,侧重于学生的分析能力和实验能力的考查,为高考常见题型,注意相关知识的学习与积累,难度不大.

练习册系列答案
相关题目
下列水溶液中的各组离子因为发生氧化还原反应而不能大量共存的是( )
| A、Na+、Ba2+、Cl-、SO42- |
| B、Ca2+、HCO3-、C1-、K+ |
| C、Fe3+、K+、I-、H+ |
| D、H+、Cl-、Na+、CO32- |
下列关于胶体的说法中正确的是( )
| A、胶体外观不均匀 |
| B、胶体粒子能通过半透膜 |
| C、胶体不稳定,静置后容易产生沉淀 |
| D、胶体微粒做不停的无秩序运动 |
某无色溶液能和Al反应放出H2,在该溶液中可能大量共存的离子组是( )
| A、Fe2+、NO3-、Cl-、H+ |
| B、Na+、OH-、NO3-、Cl- |
| C、Na+、SO42-、HCO3-、K+ |
| D、H+、SO42-、Cl-、Fe3+ |
苹果醋是一种由苹果发酵而成的食品.苹果酸(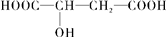 )是这种饮料的主要酸性物质.下列有关苹果酸性质的说法中,不正确的是( )
)是这种饮料的主要酸性物质.下列有关苹果酸性质的说法中,不正确的是( )
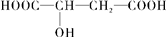 )是这种饮料的主要酸性物质.下列有关苹果酸性质的说法中,不正确的是( )
)是这种饮料的主要酸性物质.下列有关苹果酸性质的说法中,不正确的是( )| A、可以与NaHCO3溶液反应产生CO2 |
| B、可以与乙醇发生酯化反应 |
| C、1mol的苹果酸最多能与2mol金属钠反应 |
D、苹果酸与 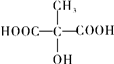 互为同分异构体 互为同分异构体 |
取pH值均等于1的盐酸和醋酸各100mL分别加水稀释到10倍后,再分别加入0.03g锌粉,在相同条件下充分反应,有关叙述正确的是( )
| A、醋酸与锌反应放出H2多 |
| B、盐酸和醋酸分别与锌反应放出的H2一样多 |
| C、醋酸与锌反应速率小 |
| D、盐酸和醋酸分别与锌反应的速率一样大 |
根据中学化学教材所附元素周期表判断,下列叙述正确的是( )
| A、M电子层电子数为奇数的所有元素都是金属 |
| B、第三、四、五、六周期元素的数目分别是8、18、32、32 |
| C、由左至右第2到12列,共十一列元素中没有非金属元素 |
| D、只有第ⅡA族元素的原子最外层有2个电子 |
已知25℃下,醋酸溶液中各微粒存在下述关系:K=1.75×10-5下列有关说法可能成立的是( )
| A、25℃条件下,向该溶液中加入一定量的盐酸时,K=8×10-5 |
| B、25℃条件下,向该溶液中加入一定量的盐酸时,K=2×10-4 |
| C、标准状况下,醋酸溶液中K=1.75×10-5 |
| D、升高到一定温度,K=7.2×10-5 |
下列基本实验操作中,正确的是( )
A、 气体除杂 |
B、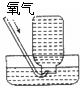 收集氧气 |
C、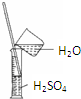 稀释溶液 |
D、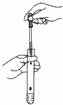 稀释溶液 |