题目内容
某不纯的铁片可能含有Mg、Al、Cu等金属杂质的一种或几种,取该铁片样品5.6g与足量的稀硫酸反应,得到标准状况下的H2 2.24L,则下列分析的结论中,正确的是( )
| A、一定同时含有三种金属杂质 |
| B、一定不含有杂质铜 |
| C、一定含有杂质镁 |
| D、可能同时含有杂质镁、铝或其中一种 |
考点:常见离子的检验方法,几组未知物的检验
专题:物质检验鉴别题
分析:根据二价金属与酸反应的化学方程式计算金属的平均式量,使平均式量介于56和另一种金属之间,以此分析解答.
解答:
解:将不纯的铁当作纯二价金属M,设其相对分子量为X,则
M~H2
X 22.4L
5.6g 2.24L
则X=56
所以一定含有铜,可能同时含有杂质镁、铝或其中一种;
故选D.
M~H2
X 22.4L
5.6g 2.24L
则X=56
所以一定含有铜,可能同时含有杂质镁、铝或其中一种;
故选D.
点评:本题考查平均相对分子量的计算,均值法在解题中的应用,避免了方程式的大量使用和计算,解题迅速方便.

练习册系列答案
相关题目
HClO4、H2SO4、HCl和HNO3都是强酸,其酸性在水溶液中差别不大.以下是某温度下这四种酸在冰醋酸中的电离常数,下列说法正确的是( )
| 酸 | HClO4 | H2SO4 | HCl | HNO3 |
| Ka | 1.6×10-5 | Ka1:6.3×10-9 | 1.6×10-9 | 4.2×10-10 |
| A、温度对这四种酸在冰醋酸中的电离常数无影响 |
| B、在冰醋酸中HClO4是这四种酸中最强的酸 |
| C、在冰醋酸中H2SO4的电离方程式为H2SO4?2H++SO42- |
| D、这四种酸在冰醋酸中都没有完全电离,所以均属于弱电解质 |
下列物质的水溶液能导电,但属于非电解质的是( )
| A、CO2 |
| B、Cl2 |
| C、NaHCO3 |
| D、NaOH |
下列四组离子中,不能在溶液中大量共存的是( )
| A、Na+、CO32-、Cl- |
| B、Ba2+、Na+、Cl- |
| C、H+、SO42-、OH- |
| D、Ag+、Al3+、NO3- |
化学与社会密不可分,利用化学反应可实现物质转化和能量转化,下列说法不正确的是( )
| A、播撒碳酸钙粉末可治理被酸雨污染的湖泊 |
| B、火力发电是将化学能直接转化为电能 |
| C、维生素C具有还原性,可消除体内具有强氧化性的物质 |
| D、过量服用阿司匹林引起酸中毒,可静脉注射NaHCO3溶液解毒 |
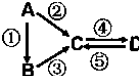 A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系:
A、B、C、D均为中学化学常见的纯净物,A是单质.它们之间有如下的反应关系: