题目内容
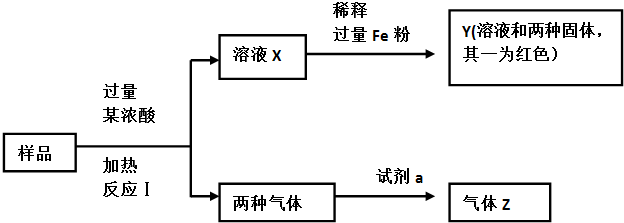
将0.2mal金属R的一种含氧酸盐在隔绝空气的条件下加热,使之完全分解,生成0.2molR的氧化物RO和CO、CO2的混合气体,已知该混合气体对氢气的相对密度为18,其体积为8.96L(标况),金属R的原子核中质子数比中子数少4个.测得RO的质量比原含氧酸盐质量减轻一半,求该盐的化学式.
考点:化学方程式的有关计算
专题:计算题
分析:先根据混合气体体积求出物质的量,混合气体对氢气的相对密度求出其混合气体的平均摩尔质量,根据m=nM求出气体质量,由RO的质量比原含氧酸盐质量减轻一半可知RO的质量与气体质量相同,然后求出RO及R的摩尔质量,推出其质子数和具体元素,利用原子守恒列式求出该盐的化学式.
解答:
解:混合气体的物质的量为:
=0.4mol,该混合气体对氢气的相对密度为18,则混合气体的平均摩尔质量为:2g/mol×18=36g/mol,
所以混合气体的质量为:m=nM=0.4mol×36g/mol=14.4g,
测得RO的质量比原含氧酸盐质量减轻一半,RO的质量与混合气体的质量相同为:14.4g,则RO的摩尔质量为:
=72g/mol,R的相对原子质量:72-16=56,
金属R的原子核中质子数比中子数少4个,则其质子数为26,即R为Fe,
该盐的式量:
=144g/mol,
设该含氧酸盐的化学式CaCxOy,则有 56+12x+16y=144,0.2x=0.4,
解得 x=2,y=4,则该盐的化学式为FeC2O4;
答:该盐的化学式为FeC2O4.
| 8.96L |
| 22.4L/mol |
所以混合气体的质量为:m=nM=0.4mol×36g/mol=14.4g,
测得RO的质量比原含氧酸盐质量减轻一半,RO的质量与混合气体的质量相同为:14.4g,则RO的摩尔质量为:
| 14.4g |
| 0.2mol |
金属R的原子核中质子数比中子数少4个,则其质子数为26,即R为Fe,
该盐的式量:
| 14.4×2g |
| 0.2mol |
设该含氧酸盐的化学式CaCxOy,则有 56+12x+16y=144,0.2x=0.4,
解得 x=2,y=4,则该盐的化学式为FeC2O4;
答:该盐的化学式为FeC2O4.
点评:本题考查了物质的量的有关计算,注意把握原子守恒在计算中的应用,题目难度中等,侧重于考查学生分析问题、解决问题的能力,以及计算能力.

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
下列叙述中正确的是( )
| A、常温下,10mlpH=12的氢氧化钠溶液中加入10mlpH=2的HA,所得溶液pH≤7 |
| B、25℃时,0.1mol/L与0.01mol/L的氯化铵溶液的pH前者大 |
| C、室温时浓度均为0.1mol/L的NH3?H2O和NH4Cl的混合液,pH为10,则,c(NH4+)+c(H+)<c(NH3?H2O)+c(OH-) |
| D、0.1mol/LNa2S溶液:c(Na+)>c(S2-)>c(HS-)>c(OH-)>c(H+) |
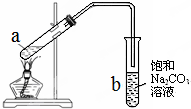 如图为实验室制取少量乙酸乙酯的装置图.下列关于该实验的叙述中,不正确的是( )
如图为实验室制取少量乙酸乙酯的装置图.下列关于该实验的叙述中,不正确的是( )| A、向a试管中先加入浓硫酸,然后边摇动试管边慢慢加入乙醇,再加冰醋酸 |
| B、实验时加热试管a的目的是及时将乙酸乙酯蒸出并加快反应速率 |
| C、试管b中Na2CO3的作用是除去随乙酸乙酯蒸出的少量乙酸和乙醇,降低乙酸乙酯在溶液中溶解度 |
| D、试管b中导气管下端管口不能浸入液面的原因是防止实验过程中发生倒吸现象 |
实验室用以下三种途径来制取相同质量的硝酸铜:从消耗原料和是否污染环境的角度,下列有关叙述不正确的是( )
①铜与浓硝酸反应;②铜与稀硝酸反应;③铜与氧气反应生成CuO,CuO再与稀硝酸反应.
①铜与浓硝酸反应;②铜与稀硝酸反应;③铜与氧气反应生成CuO,CuO再与稀硝酸反应.
| A、所消耗的铜的质量相等 |
| B、所消耗的硝酸的量:②>①>③ |
| C、对环境造成的危害,③最小 |
| D、制取硝酸铜的最佳方案是③ |
镁铝合金5.1g溶于300mL 2mol?L-1盐酸中,标准状况下放出气体体积为5.6L,向反应后的溶液中加入500mL NaOH溶液充分反应,最终产生白色沉淀.下列有关说法不正确的是( )
| A、5.1 g镁铝合金中含有镁、铝的质量分别为2.4 g、2.7 g |
| B、溶解5.1 g镁铝合金时,剩余盐酸的物质的量为0.1 mol |
| C、生成白色沉淀的最大质量为13.6 g |
| D、若白色沉淀只有Mg(OH)2,该NaOH溶液的物质的量浓度至少为1.2 mol?L-1 |
C5H12有3种不同结构:甲、CH3( CH2 )3CH3,乙、CH3CH (CH3 ) CH2CH3,丙、C(CH3)4.下列相关叙述正确的是( )
| A、甲、乙、丙属同系物,均可与氯气发生取代反应 |
| B、甲的分子中所有碳原子在同一直线上 |
| C、甲、乙、丙中,丙的沸点最低 |
| D、丙有3种不同沸点的二氯取代物 |