题目内容
17.某研究小组为了探究一种无机矿物盐X(仅含Ca、Fe、C、O四种元素)的组成和性质,设计并完成了如下实验: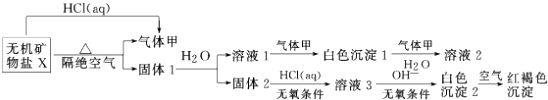
(1)流程图中红褐色沉淀是Fe(OH)3,白色沉淀2是Fe(OH)2,由白色沉淀2转化成红褐色沉淀的化学方程式为4Fe(OH)2+2H2O+O2=4Fe(OH)3.
(2)固体2的成分为FeO,写出固体2与盐酸反应的离子方程式FeO+2H+=Fe2++H2O.
(3)在酸性条件下,H2O2能将Fe2+氧化成Fe3+,反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.
(4)溶液3中含有金属阳离子是Fe2+,如何通过实验检验该离子的存在将样品溶解,先滴加硫氢化钾溶液,无现象,再加氯水,则溶液变血红色,说明含有二价铁离子.
(5)气体甲的成分是CO2,气体甲与固体2在一定条件下可以发生氧化还原反应,写出此反应的化学方程2FeO+CO2$\frac{\underline{\;一定条件\;}}{\;}$Fe2O3+CO(或生成Fe3O4).
分析 无机矿物盐X(仅含Ca、Fe、C、O四种元素),和HCl(aq)反应生成气体甲,因此猜测X是碳酸盐,X加热易分解且能和酸反应生成CO2,那么甲为CO2,固体1为金属氧化物,溶于水得到溶液1和固体2,溶液1和二氧化碳反应生成白色沉淀1,白色沉淀1和二氧化碳、水反应生成溶液2,则白色沉淀1为碳酸盐、溶液2为碳酸氢盐;
固体2和稀盐酸反应生成溶液3,且需要无氧条件,溶液3中加入碱在无氧条件下生成白色沉淀2,白色沉淀2被空气氧化生成红褐色沉淀,则白色沉淀2是Fe(OH)2,溶液3为FeCl2,则固体2为FeO,X仅含4种元素,碳酸盐分解生成二氧化碳气体和两种氧化物,其中一种氧化物能溶于水,结合地壳的成分猜测固体1中成分为CaO、FeO,对应地,X应为CaFe(CO3)2,那么溶液1是Ca(OH)2,白色沉淀1是CaCO3,溶液2是Ca(HCO3)2,再结合题目分析解答.
解答 解:无机矿物盐X(仅含Ca、Fe、C、O四种元素),和HCl(aq)反应生成气体甲,因此猜测X是碳酸盐,X加热易分解且能和酸反应生成CO2,那么甲为CO2,固体1为金属氧化物,溶于水得到溶液1和固体2,溶液1和二氧化碳反应生成白色沉淀1,白色沉淀1和二氧化碳、水反应生成溶液2,则白色沉淀1为碳酸盐、溶液2为碳酸氢盐;
固体2和稀盐酸反应生成溶液3,且需要无氧条件,溶液3中加入碱在无氧条件下生成白色沉淀2,白色沉淀2被空气氧化生成红褐色沉淀,则白色沉淀2是Fe(OH)2,溶液3为FeCl2,则固体2为FeO,X仅含4种元素,碳酸盐分解生成二氧化碳气体和两种氧化物,其中一种氧化物能溶于水,结合地壳的成分猜测固体1中成分为CaO、FeO,对应地,X应为CaFe(CO3)2,那么溶液1是Ca(OH)2,白色沉淀1是CaCO3,溶液2是Ca(HCO3)2,(1)通过以上分析知,红褐色沉淀是Fe(OH)3,白色沉淀2是Fe(OH)2,氢氧化亚铁不稳定,易被空气氧化生成红褐色氢氧化铁,所以白色沉淀2在空气中变成红褐色沉淀,反应方程式为4Fe(OH)2+2H2O+O2=4Fe(OH)3;
故答案为:Fe(OH)3;Fe(OH)2;4Fe(OH)2+2H2O+O2=4Fe(OH)3;
(2)固体2的成分为FeO,FeO与盐酸反应的离子方程式FeO+2H+=Fe2++H2O,故答案为:FeO+2H+=Fe2++H2O;
(3)在酸性条件下,H2O2能将Fe2+氧化成Fe3+,反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O,故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
(4)根据以上分析,溶液3为FeCl2溶液,含有金属阳离子是Fe2+,检验含有二价铁,可将样品溶解,先滴加硫氢化钾溶液,无现象,再加氯水,则溶液变血红色,说明含有二价铁;故答案为:Fe2+;将样品溶解,先滴加硫氢化钾溶液,无现象,再加氯水,则溶液变血红色,说明含有二价铁离子;
(5)根据以上分析,气体甲的成分是CO2,固体2为FeO,气体甲与固体2在一定条件下可以发生氧化还原反应,氧化亚铁具有还原性,能被二氧化碳氧化生成四氧化三铁或氧化铁,同时生成CO,反应方程式为2FeO+CO2$\frac{\underline{\;一定条件\;}}{\;}$Fe2O3+CO(或生成Fe3O4),故答案为:CO2;2FeO+CO2$\frac{\underline{\;一定条件\;}}{\;}$Fe2O3+CO(或生成Fe3O4).
点评 本题考查了无机物推断,涉及物质结构、物质的性质、离子的检验等知识点,熟悉元素化合物的性质是解本题关键,知道流程图中每一步发生的反应及反应现象,题目难度中等.

| A. | 22.4L氢气中含有氢分子数目为NA | |
| B. | 常温常压下,14g氮气含有的原子数目为NA | |
| C. | 0.5mol Na2CO3中含有的Na+数目为0.5NA | |
| D. | 0.5mol/L Fe2(SO4)3溶液中,SO42-的数目为1.5NA |
| A. | 为测定熔融氢氧化钠的导电性,可在氧化铝坩埚中熔化氢氧化钠固体后进行测量 | |
| B. | Fe(OH)3胶体可以将Fe Cl3滴入NaOH溶液中进行制备 | |
| C. | 除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤 | |
| D. | 某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中一定含有CO32- |
| A. | ④③①⑤② | B. | ④⑤①③② | C. | ①⑤③④② | D. | ③④①⑤② |
| A. | 石墨作阳极,铁作阴极 | |
| B. | 粗铜(含Fe、Ni、Zn)作阳极,纯铜作阴极 | |
| C. | 纯铜作阳极,铁作阴极 | |
| D. | 铁作阳极,纯铜作阴极 |
| A. | PCl5 | B. | SO2 | C. | BF3 | D. | CS2 |