题目内容
1.工业上曾经通过反应“3Fe+4NaOH$\stackrel{1100℃}{?}$Fe3O4+2H2↑4Na↑”生产金属钠,己知铁的熔点1535℃、沸点3000℃.下列有关说法正确的是( )| A. | 增大铁的量可以使反应速率加快 | |
| B. | 将生成的气体在空气中冷却可获得钠 | |
| C. | 每生成1molH2,转移的电子数约为4×6.02×1023 | |
| D. | 该反应条件下铁的金属性比钠强 |
分析 A、铁为固体,增大铁的量,反应速率不变;
B、钠极易被空气中的氧气氧化;
C、每生成1molH2,转移的电子为4mol;
D、该反应条件下铁的还原性比钠强.
解答 解:A、铁为固体,增大铁的量,反应速率不变,故A错误;
B、钠极易被空气中的氧气氧化,所以将生成的气体在空气中冷却得不到钠,故B错误;
C、每生成1molH2,转移的电子为4mol即转移的电子数约为4×6.02×1023,故C正确;
D、该反应条件下铁的还原性比钠强,而不是金属性,故D错误;
故选C.
点评 本题考查氧化还原反应,明确元素化合价变化是解本题关键,难度不大.

练习册系列答案
相关题目
关于原电池和电解池的叙述正确的是( )
A.原电池中失去电子的电极为正极
B.原电池的负极、电解池的阳极都发生氧化反应
C.原电池的两极一定是由活动性不同的两种金属组成
D.电解时电解池的阴极一定是阴离子放电
12.将两个铂电极插入KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池.已知.通入CH4的一极,其电极反应式是:CH4+10OH--8e-═CO32-+7H2O;通入O2的另一极,其电极反应式是:2O2+4H2O+8e-═8OH-下列叙述正确的( )
| A. | 通入CH4的电极为负极 | |
| B. | 负极发生氧化反应 | |
| C. | 该电池使用一段时间后无需补充KOH | |
| D. | 燃料电池工作时,溶液中的OH-向正极移动 |
9.与50mL 0.1mol•L-1 Na2CO3 溶液中 Na+ 的物质的量浓度相同的溶液是( )
| A. | 50 mL 0.2 mol•L-1 的 NaCl 溶液 | |
| B. | 100 mL 0.1 mol•L-1 的 NaCl 溶液 | |
| C. | 25 mL 0.2 mol•L-1 的 Na2SO4 溶液 | |
| D. | 10 mL 0.5mol•L-1 的 Na2CO3 溶液 |
6.下列各组物质中,第一种是酸,第二种是混合物,第三种是碱的是( )
| A. | 空气、硫酸铜、H2SO4 | B. | HCl、Fe(OH)3胶体、纯碱 | ||
| C. | 二氧化碳、胆矾、氢氧化钾 | D. | HNO3、食盐水、烧碱 |
13.用NA表示阿伏德罗常数,下列叙述正确的是( )
| A. | 标准状况下,22.4LCCl4含有的分子数为1 NA | |
| B. | 常温常压下,16g O2含有的原子数为1 NA | |
| C. | 通常状况下,1 NA 个CO2分子占有的体积为22.4L | |
| D. | 物质的量浓度为0.5mol/L的BaCl2溶液中,含有Cl- 个数为1 NA |
10.下列饱和溶液中,通入过量二氧化碳气体,肯定没有沉淀产生的是( )
①氢氧化钠
②碳酸钠
③硅酸钠
④次氯酸钙
⑤氯化钙.
①氢氧化钠
②碳酸钠
③硅酸钠
④次氯酸钙
⑤氯化钙.
| A. | ①⑤ | B. | ①② | C. | ④⑤ | D. | ③④ |
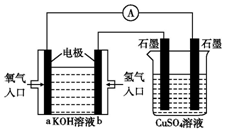 可用碱性氢氧燃料电池组装如图所示的装置:
可用碱性氢氧燃料电池组装如图所示的装置: 4X(g) + nY(g)达到平衡后,容器温度不变,混合气体的压强是原来的87.5%,则化学方程式中的n值为( )
4X(g) + nY(g)达到平衡后,容器温度不变,混合气体的压强是原来的87.5%,则化学方程式中的n值为( )